题目内容
【题目】一定温度下,将4molNH3和5molO2充入定容密闭容器中,在催化剂存在下进行下列反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H=- 1025 kJ/mol,当达到平衡状态时,下列说法中正确的是
4NO(g)+6H2O(g) △H=- 1025 kJ/mol,当达到平衡状态时,下列说法中正确的是
A. 生成4molNO B. NH3和NO物质的量之和为4mol
C. 放出1025kJ的热量 D. 平衡时容器内气体压强和开始时压强相等
【答案】B
【解析】A. 该反应为可逆反应,不能完全转化,因此生成的NO 少于4mol ,故A错误;B. 根据N原子守恒,NH3和NO物质的量之和为4mol,故B正确;C. 该反应为可逆反应,放出的热量少于1025kJ,故C错误;D. 该反应恰好气体的物质的量增大,平衡时容器内气体压强大于开始时压强,故D错误;故选B。

练习册系列答案
相关题目
【题目】从某含Br—废水中提取Br2的过程包括:过滤、氧化、萃取(需选择合适萃取剂)及蒸馏等步骤。已知:
物质 | Br2 | CCl4 | 正十二烷 |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |
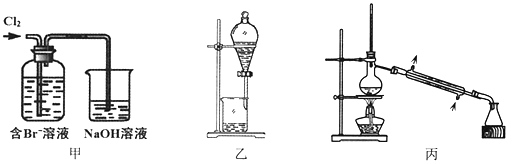
下列说法不正确的是
A. 甲装置中Br—发生的反应为:2Br-+ Cl2 = Br2 + 2Cl-
B. 甲装置中NaOH溶液每吸收0.1mol Cl2,转移0.1mol e—
C. 用乙装置进行萃取,溶解Br2的有机层在下层
D. 用丙装置进行蒸馏,先收集到的是Br2