题目内容
【题目】设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
 NaCl晶胞
NaCl晶胞
A.124g P4含有的P-P键数为6NA
B.12g石墨中含有的C-C键数为2NA
C.58.5g NaCl中晶胞数为NA
D.12g金刚石中含有的C-C键数为1.5NA
【答案】A
【解析】
A. 124g白磷中含有的磷分子个数=![]() ×NA/mol=NA,一个白磷分子中含有6个P-P键,所以124g P4含有的P-P键的个数为6NA,故A正确;
×NA/mol=NA,一个白磷分子中含有6个P-P键,所以124g P4含有的P-P键的个数为6NA,故A正确;
B. 12g石墨中含有碳原子个数=![]() ×NA/mol=NA,石墨中每个碳原子含有
×NA/mol=NA,石墨中每个碳原子含有![]() 个C-C键,所以12g石墨中含有C-C键个数是1.5NA,故B错误;
个C-C键,所以12g石墨中含有C-C键个数是1.5NA,故B错误;
C. 58.5 g NaCl的物质的量为![]() =1mol,根据晶胞示意图可知每个晶胞中含有4个Na+和4个Cl-,所以1mol NaCl所含晶胞的物质的量为0.25mol,数目为0.25NA,故C错误;
=1mol,根据晶胞示意图可知每个晶胞中含有4个Na+和4个Cl-,所以1mol NaCl所含晶胞的物质的量为0.25mol,数目为0.25NA,故C错误;
D. 12g金刚石中含有碳原子个数=![]() ×NA/mol=NA,金刚石中每个碳原子含有2个C-C键,所以12g金刚石中含有C-C键个数是2NA,故D错误;
×NA/mol=NA,金刚石中每个碳原子含有2个C-C键,所以12g金刚石中含有C-C键个数是2NA,故D错误;
故答案为A。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案【题目】化学反应速率和限度与生产、生活密切相关。
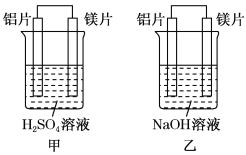
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气标准状况,实验记录如表累计值:
时间 | 1 | 2 | 3 | 4 | 5 |
氢气体积 | 100 | 240 | 464 | 576 | 620 |
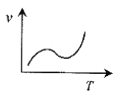
①哪一时间段反应速率最大__(填0~1、1~2、2~3、3~4、4~5min)。反应开始后反应速率先增大的原因是__。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率___(设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入少量的下列溶液以减慢反应速率,你认为不可行的是__。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是__。
②该反应达到平衡状态的标志是__。
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变
D.生成2mol Z的同时生成3mol X