��Ŀ����
����Ŀ���ش������й����⡣
��1��ij��ҵ��ˮ�н����±������е�5��(������ˮ�ĵ��뼰���ӵ�ˮ��)���Ҹ������ӵ����ʵ���Ũ����ȣ���Ϊ0.1mol/L��
������ | K�� | Cu2�� | Fe3�� | Al3�� | Fe2�� |
������ | Cl�� | CO32�� | NO3�� | SO42�� | SiO32�� |
ijͬѧ��̽����ˮ����ɣ�����������ʵ�飺
���ò�˿պȡ������Һ���ڻ��������գ�����ɫ����(����ɫ�ܲ����۲�)��
��ȡ������Һ������KSCN��Һ�����Ա仯��
����ȡ��Һ�����������ᣬ����ɫ�������ɣ�����ɫ������������ɺ���ɫ����ʱ��Һ��Ȼ���壬����Һ������������䡣
������������õ���Һ�м���BaCl2��Һ���а�ɫ�������ɡ�
���ƶϣ�ԭ��Һ��������������___________________����������_____________________��
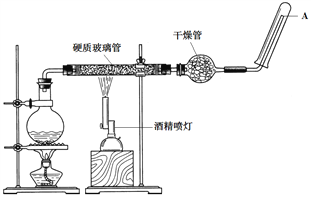
��2����������ǵ�����������̫��������Ҫ��ʽ֮һ��ͼ1Ϊ�����������װ�ã�ͼ2Ϊ�������[CO(NH2)2]�ļ�����Һ�����װ��ʾ��ͼ(�����и�Ĥ����ֹ����ͨ��������������Ϊ���Ե缫)��

ͼ1 ͼ2
��ͼ1��N�Ͱ뵼��Ϊ____________(�������������)
�ڸ�ϵͳ����ʱ��A���ĵ缫��ӦʽΪ___________________________________________��
����A������7.00gN2�����ʱB������_____________LH2(��״����)��
���𰸡�Fe2����Cu2��Cl����NO3����SO42������CO(NH2)2��8OH����6e���TCO32����N2����6H2O16.8
��������
(1)���ò�˿պȡ������Һ���ڻ��������գ�����ɫ����(����ɫ�ܲ����۲�)��˵��û��K+����ȡ������Һ������KSCN��Һ�����Ա仯��˵��û��Fe3+������ȡ��Һ�����������ᣬ����ɫ�������ɣ�����ɫ������������ɺ���ɫ����ʱ��Һ��Ȼ���壬����Һ������������䣬˵�� Fe2+��NO3-��H+��Ӧ����NO������Һ����Fe2+��NO3-����������Һ������������䣬˵��ԭ��Һ����Cl-����������Һ��Ȼ���壬˵��û��SiO32-��������������õ���Һ�м���BaCl2��Һ���а�ɫ�������ɣ�˵����SO42-���������ƶϿ�֪��Һ��������Ϊ Cl-��NO3-��SO42-���Ҹ�Ϊ0.1mol/L���Ѿ��ƶϳ�����������Fe2+����Ũ��Ϊ0.1mol/L���ɵ���غ��֪��Һ�л���һ��+2�������ӣ����Ի���Cu2+�����Լ�ͬѧ����ȷ��ԭ��Һ�������������ǣ�Fe2+��Cu2+���������ǣ�Cl-��NO3-��SO42-���ʴ�Ϊ��Fe2+��Cu2+��Cl-��NO3-��SO42-��
(2)�ٸõ�ط�Ӧʱ�У���Ԫ�ػ��ϼ���-3�۱�Ϊ0�ۣ�HԪ�ػ��ϼ���+1�۱�Ϊ0�ۣ���Ԫ�ر���������Ԫ�ر���ԭ���������ɵ����ĵ缫A�����������������ĵ缫B����������ͼ1��N�Ͱ뵼��Ϊ������P�Ͱ뵼��Ϊ�������ʴ�Ϊ��������
��A��Ϊ�������缫��ӦʽΪ��CO(NH2)2+80H--6e-�TCO32-+N2��+6H2O���ʴ�Ϊ��CO(NH2)2+8OH--6e-�TCO32-+N2��+6H2O��
��A��Ϊ�������缫��ӦʽΪ��CO(NH2)2+80H--6e-�TCO32-+N2��+6H2O����A������7.00g N2����0.25molN2����ת�Ƶ�����1.5mol����ʱB������������B�缫��ӦΪ��2H2O+2e-�TH2��+2OH-��ת��1.5mol���ӣ����������������![]() ��22.4L/mol=16.8L���ʴ�Ϊ��16.8��
��22.4L/mol=16.8L���ʴ�Ϊ��16.8��

����Ŀ������ͼװ���о��绯ѧԭ�������з����д������

ѡ�� | ���� | �缫���� | ���� | |
a | b | |||
A | K1K2 | ʯī | �� | ģ������������ʴ |
B | K1K2 | п | �� | ģ������������������������������� |
C | K1K3 | ʯī | �� | ģ���ⱥ��ʳ��ˮ |
D | K1K3 | �� | ʯī | ģ�������������ӵ��������������� |
A. A B. B C. C D. D
����Ŀ��SO2��һ����Ҫ��������,���������������������ᡢ�������Ρ����������,Ҳ������Ѭ������������������������ԭ���ȡ�
(1)SO2���ʶ��,����SO2����ͨ����������,�ܿ���������Ϊ:__________,�÷�Ӧ��SO2���ֳ�______��;����SO2����ͨ�����Ը��������Һ��,���ӷ�Ӧ����ʽΪ_________,�÷�Ӧ��SO2���ֳ�__________�ԡ�
(2)SO2�ж�,�����γ�����,�Ǵ�����Ҫ��Ⱦ��֮һ��ʯ��-ʯ�෨�ͼ�dz��õ���������ʯ��-ʯ�෨������ԭ��:��SO2+Ca(OH)2=CaSO3��+H2O��2CaSO3+O2+4H2O=2CaSO4��2H2O�������ԭ��:����SO2��β��ͨ���������ռ���Һ��,��д����Ӧ�Ļ�ѧ��Ӧ����ʽ__________;
��֪:
�Լ� | Ca(OH)2 | NaOH |
�۸�(Ԫ/kg) | 0.36 | 2.9 |
��ʯ��-ʯ�෨���,����ŵ������տ졢Ч�ʸ�,ȱ����__________;
(3)��ʯ��-ʯ�෨�ͼ�Ļ�����,�����˫�,��ʵ������ѭ�����á�

����������,ʵ��ѭ�����õ�������__________,���û�ѧ����ʽ��ʾ��Na2SO3��Һ�м���CaO��ķ�Ӧԭ��__________��