题目内容
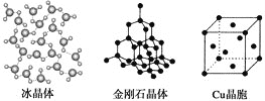
【题目】现有一种蓝色晶体,可表示为MxFey(CN)6,经X 射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上。其晶体中阴离子的最小结构单元如下图所示。下列说法中正确的是( )

A. 该晶体的化学式为MFe2(CN)6
B. 该晶体属于离子晶体,M呈+3价
C. 该晶体属于离子晶体,M呈+2价
D. 晶体中与每个Fe3+距离最近且等距离的CN-为3个
【答案】A
【解析】
Fe3+和Fe2+互相占据立方体互不相邻的顶点,则该结构单元中,所含Fe3+有![]() 个,Fe2+有
个,Fe2+有![]() 个,CN-有
个,CN-有![]() 个。由于该晶体的化学式为MxFey(CN)6,所以y=2,且该晶体的化学式中含有1个Fe3+、1个Fe2+,所以x为1,即该化学式为MFe2(CN)6。
个。由于该晶体的化学式为MxFey(CN)6,所以y=2,且该晶体的化学式中含有1个Fe3+、1个Fe2+,所以x为1,即该化学式为MFe2(CN)6。
A. 经计算得知,该结构单元中,含有![]() 个Fe2+、
个Fe2+、![]() 个Fe3+、3个CN-。由于该晶体的化学式为MxFey(CN)6,则y=2,x=1,即该化学式为MFe2(CN)6,A正确;
个Fe3+、3个CN-。由于该晶体的化学式为MxFey(CN)6,则y=2,x=1,即该化学式为MFe2(CN)6,A正确;
B. 从构成晶体的微粒来看,该晶体为离子晶体;由于化学式为MFe2(CN)6,M呈+1价,B错误;
C. 该晶体为离子晶体;由于化学式为MFe2(CN)6,M呈+1价,C错误;
D. 晶体中与每个Fe3+距离最近且等距离的CN-为6个,D错误;
故合理选项为A。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】根据所学知识回答下列问题。
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.单位质量的![]() 和
和![]() 单质燃烧时均放出大量热,可用作燃料.已知
单质燃烧时均放出大量热,可用作燃料.已知![]() 和
和![]() 为短周期元素,其原子的第一至第四电离能如下表所示:
为短周期元素,其原子的第一至第四电离能如下表所示:
电离能/ |
|
|
|
|
| 932 | 1821 | 15390 | 21771 |
| 738 | 1451 | 7733 | 10540 |
①某同学根据上述信息,推断![]() 的核外电子排布如图所示,该同学所画的电子排布图违背了_________,
的核外电子排布如图所示,该同学所画的电子排布图违背了_________, ![]() 元素位于周期表五个区域中的___ 区。
元素位于周期表五个区域中的___ 区。

②![]() 分子的中心原子
分子的中心原子![]() 采取_________杂化,
采取_________杂化, ![]() 的空间构型为___ 。
的空间构型为___ 。
(2)![]() 原子或离子外围有较多能量相近的空轨道,所以其能与一些分子或离子形成配合物。
原子或离子外围有较多能量相近的空轨道,所以其能与一些分子或离子形成配合物。
① 与![]() 原子或离子形成配合物的分子或离子应具备的结构特征是____。
原子或离子形成配合物的分子或离子应具备的结构特征是____。
② 六氰合亚铁离子![]() 中不存在____________(填字母)。
中不存在____________(填字母)。
A.共价键 B.非极性键 C.配位键 D. ![]() 键
键
写出一种与![]() 互为等电子体的单质的分子式:________________ 。
互为等电子体的单质的分子式:________________ 。
(3)—种![]() 合金的晶胞结构如图,请据此回答下列问题:
合金的晶胞结构如图,请据此回答下列问题:
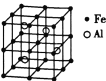
① 该合金的化学式为____________。
② 若晶体的密度为![]()
![]() ,则该晶胞棱长为____________
,则该晶胞棱长为____________![]() (设
(设![]() 为阿伏加德罗常数的值,用含
为阿伏加德罗常数的值,用含![]() 和
和![]() 的代数式表示,不必化简)。
的代数式表示,不必化简)。