题目内容
6.下列物质:①Na ②Na2O ③NH3④HCl ⑤Ba(OH)2 ⑥NaCl⑦蔗糖 ⑧NaCl溶液.(填序号)(1)属于电解质的是②④⑤⑥,
(2)属于非电解质的是③⑦,
(3)能导电的是①⑧.
分析 物质导电的原因:含有自由移动的离子或自由电子;
电解质是在水溶液里或熔融状态下能导电的化合物,包括酸、碱、盐、活泼金属氧化物和水;
非电解质是在水溶液里和熔融状态下都不能导电的化合物,包括一些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等);据此解答.
解答 解:①Na是金属单质,含有自由电子,能够导电;既不是电解质也不是非电解质;
②Na2O 是金属氧化物,不含有自由移动的离子或自由电子,不导电;熔融状态下能导电的化合物,是电解质;
③NH3,不含有自由移动的离子或自由电子,不导电;本身不能电离产生离子,属于非电解质;
④HCl不含有自由移动的离子或自由电子,不导电;在水溶液里能导电的化合物,是电解质;
⑤Ba(OH)2 不含有自由移动的离子或自由电子,不导电;在水溶液里或熔融状态下能导电的化合物,是电解质;
⑥NaCl不含有自由移动的离子或自由电子,不导电;在水溶液里或熔融状态下能导电的化合物,是电解质;
⑦蔗糖不含有自由移动的离子或自由电子,不导电;在水溶液里和熔融状态下都不能导电的化合物,是非电解质;
⑧NaCl溶液含有自由移动的离子,能够导电;属于混合物,既不是电解质也不是非电解质;
所以属于电解质的有:②④⑤⑥;属于非电解质的有:③⑦;能导电的是:①⑧;
故答案为:(1)②④⑤⑥
(2)③⑦
(3)①⑧.
点评 本题考查了电解质溶液导电的原因及电解质、非电解质的判断,熟悉相关概念是解题关键,注意单质、混合物既不是电解质,也不是非电解质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.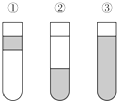 在盛有溴水的三支试管中分别加入苯、四氯化碳和酒精,振荡后静置,出现如图所示的现象,正确的结论是( )
在盛有溴水的三支试管中分别加入苯、四氯化碳和酒精,振荡后静置,出现如图所示的现象,正确的结论是( )
 在盛有溴水的三支试管中分别加入苯、四氯化碳和酒精,振荡后静置,出现如图所示的现象,正确的结论是( )
在盛有溴水的三支试管中分别加入苯、四氯化碳和酒精,振荡后静置,出现如图所示的现象,正确的结论是( )| A. | ①加CCl4 ②加苯 ③加酒清 | B. | ①加酒精 ②加CCl4 ③加苯 | ||
| C. | ①加苯 ②加CCl4 ③加酒精 | D. | ①加苯 ②加酒精 ③加CCl4 |
17.下列指定反应的离子方程式正确的是( )
| A. | MnO2与浓盐酸混合加热:MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| B. | (NH4)2Fe(SO4)2溶液中加入过量的NaOH溶液:Fe2++2OH-=Fe(OH)2↓ | |
| C. | Ba(HCO3)2溶液中加入稀硫酸:Ba2++SO${\;}_{4}^{2-}$=BaSO4↓ | |
| D. | H2C2O4(弱酸)溶液中加入酸性KMnO4溶液:2MnO${\;}_{4}^{-}$+5H2C2O4=2Mn2++10CO2↑+2H2O+6OH- |
1.下列离子方程式正确的是( )
| A. | 澄清的石灰水与盐酸反应 Ca(OH)2+2H+=Ca2++2H2O | |
| B. | 钠与水的反应 Na+2H2O=Na++2OH-+H2↑ | |
| C. | 铜片插入硝酸银溶液 Cu+Ag+=Cu2++Ag | |
| D. | 大理石溶于醋酸CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
18.V mL硫酸铝溶液中,含Al3+m g,取V/4mL该溶液稀释到4VmL,则稀释后溶液中SO42-的物质的量浓度为( )
| A. | 125m/9V mol/L | B. | 125m/18 V mol/L | ||
| C. | 125 m/36V mol/L | D. | 125 m/54V mol/L |
15.下列说法正确的是( )
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子 | |
| B. | 强电解质溶液不一定比弱电解质溶液的导电性强 | |
| C. | 盐酸、氢氧化钠、硫酸钡和氧化铝一定是强电解质 | |
| D. | 强、弱电解质的导电性由溶液中溶质的浓度决定 |
16.能正确表示下列化学反应的离子方程式的是( )
| A. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O | |
| B. | 饱和氢氧化钙溶液与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O | |
| C. | 在氢氧化钡溶液中加入少量小苏打:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O | |
| D. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O |