题目内容
【题目】反应 Fe(s)+CO2(g)FeO(s)+CO(g) △H1,平衡常数为 K1,反应 Fe(s)+H2O(g)FeO(s)+H2(g) △H2,平衡常数为 K2;在不同温度时 K1、K2 的值如表:
700℃ | 900℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
(1) 反应 CO2(g)+H2(g)CO(g)+H2O(g)的反应热为△H ,平衡常数为 K,则△H= ____________(用△H1 和△H2 表 示), K= _______________ (用 K1 和 K2 表示),且由上述计算可知,反应CO2(g)+H2(g)CO(g)+H2O(g)是______________________________反应(填“吸热”或“放热”)。
(2) 现有反应:mA(g)+nB(g) pC(g)达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
①该反应的逆反应为反应___________(填“吸热”或“放热”,且 m+n___p(填“>"“=或“<”)
②减压使容器容积增大时,A的质量分数____________(填“增大”“减小”或“不变”,下同)。
③若容积不变加入B,则A的转化率_______________, B的转化率 ______________
④ 若加入催化剂,平衡时气体混合物的总物质的量____________
【答案】ΔH1-ΔH2 ![]() 吸热 放热 > 增大 增大 减小 不变
吸热 放热 > 增大 增大 减小 不变
【解析】
(1)据已知热化学方程式,利用盖斯定律解答;据化学平衡常数表达式分析;
(2)达到平衡后,当升高温度时,B的转化率变大,说明温度升高平衡向正反应方向移动,则正反应吸热,当减小压强时,混合体系中C的质量分数也减小,说明压强减小平衡向逆反应方向移动,则方程式中反应物的气体的计量数之和大于生成物气体的化学计量数之和,根据外界条件对化学平衡的影响解答该题。
(1)①已知①Fe(s)+CO2(g)FeO(s)+CO(g)△H1,②Fe(s)+H2O(g)FeO(s)+H2(g)△H2,据盖斯定律,①-②得:CO2(g)+H2(g)CO(g)+H2O(g)△H=△H1-△H2;反应的K=![]() ,K1=
,K1=![]() ,K2=
,K2=![]() ,所以K=
,所以K=![]() ;根据表中数据,700℃时,K<1,900℃时,K>1,所以温度升高,K增大,平衡右移,说明该反应的正反应是吸热反应;
;根据表中数据,700℃时,K<1,900℃时,K>1,所以温度升高,K增大,平衡右移,说明该反应的正反应是吸热反应;
(2)①达到平衡后,当升高温度时,B的转化率变大,说明温度升高平衡向正反应方向移动,则正反应吸热,逆反应为放热反应,当减小压强时,混合体系中C的质量分数也减小,说明压强减小平衡向逆反应方向移动,则方程式中反应物的气体的计量数之和大于生成物气体的化学计量数之和,
故答案为:放热;>;
②减压,平衡向着方程式中气体的计量数之和增大的反应方向移动,即向着逆反应方向移动,则A的质量分数增大,故答案为:增大;
③在反应容器中加入一定量的B,反应物B的浓度增大,平衡向正反应方向移动,促进A的转化,A的转化率增大,但B的转化率减小,故答案为:增大;减小;
④催化剂对化学平衡移动没有影响,所以若加入催化剂,平衡时气体混合物的总物质的量不变。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】为了减轻汽车尾气造成的大气污染,人们开始探索利用 NO 和 CO 在一定条件下 转化为 两种无毒气体E和F的方法(已知该反应△H<0). 在2L密闭容器中加入一定量 NO和CO,当温度分别在 T1 和 T2 时,测得各物质平衡时物质的量如下表:
n(mol) | NO | CO | E | F |
初始 | 0.100 | 0.100 | 0 | 0 |
T1 | 0.020 | 0.020 | 0.080 | 0.040 |
T2 | 0.010 | 0.010 | 0.090 | 0.045 |
(1)请结合上表数据,写出 NO 与 CO 反应的化学方程式_________________________________。
(2)根据表中数据判断,温度T1和T2的关系是(填序号)__________。
A.T1>T2 B. T1<T2 C. T1=T2 D.无法比较
(3)已知:4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g) ΔH=- 1266.8 kJ/mol,N2(g) + O2(g) = 2NO(g) ΔH = + 180.5kJ/mol,则氨催化氧化的热化学方程式为:________________________。
(4)500℃下,在 A、B 两个容器中均发生合成氨的反应。隔板Ⅰ固定不动,活塞Ⅱ可自由移动。
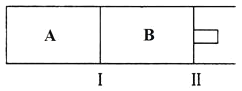
当合成氨在容器 B 中达平衡时,测得其中含有 1.0molN2,0.4molH2,0.4molNH3,此时容积为2.0L。则此条件下的平衡常数为_______________;保持温度和体积不变,向此容器中通入0.36molN2,平衡将__________________(填“正向”、“逆向”或“不”)移动。