题目内容
【题目】某学生验证浓硫酸性质的实验如图。下列叙述错误的是
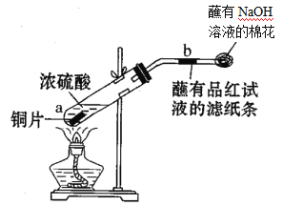
A.反应一段时间后,b处滤纸条褪色
B.蘸有NaOH溶液的棉花团作用是吸收多余的SO2,防止污染空气
C.化学反应方程式:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O
D.硫酸型酸雨形成的可能原因是:SO2+H2O![]() H2SO3;O2+2H2SO3=2H2SO4
H2SO3;O2+2H2SO3=2H2SO4
【答案】C
【解析】
A.Cu与浓硫酸混合加热发生反应:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,产生的SO2气体具有漂白性,能够使b处蘸有品红溶液的试纸褪色,A正确;
CuSO4+SO2↑+2H2O,产生的SO2气体具有漂白性,能够使b处蘸有品红溶液的试纸褪色,A正确;
B.NaOH是碱,能够与酸性氧化物SO2反应产生盐,因此蘸有NaOH溶液的棉花团可以吸收多余的SO2,防止污染空气,B正确;
C.Cu与浓硫酸反应需在加热条件下进行,若不加热,不具备反应条件,反应不能发生,C错误;
D.硫酸型酸雨形成的原因是:SO2与空气中的水反应产生H2SO3,H2SO3具有强的还原性,与O2反应产生H2SO4,反应方程式为:SO2+H2O![]() H2SO3;2H2SO3+O2=2H2SO4,D正确;
H2SO3;2H2SO3+O2=2H2SO4,D正确;
故合理选项是C。

【题目】“笔、墨、纸、砚”在中国传统文化中被称为“文房四宝”,下列说法中错误的是( )
A | B | C | D |
|
|
|
|
用灼烧法可鉴别羊毫与尼龙毫的真伪 | 墨的主要成分是碳单质 | 纸的主要成分属于合成材料 | 用石材制作砚台的过程是物理变化 |
A.AB.BC.CD.D
【题目】依据下列实验现象,得出的结论正确的是
操作 | 实验现象 | 结论 | |
A | 向NaBr 溶液中加入过量氯水,再加入淀粉 KI 溶液 | 最终溶液变蓝 | 氧化性:Cl2>Br2>I2 |
B | 向某无色溶液中滴加浓盐酸 | 产生能使品红溶液褪色的气体 | 不能证明原溶液中含有SO32-或HSO3- |
C | 向蔗糖溶液中加入稀硫酸,水浴加热后, 加入新制氢氧化铜,加热 | 得到蓝色溶液 | 蔗糖水解产物没有还原性 |
D | 向2mL 0.01mol/L的AgNO3溶液中滴加几滴同浓度的NaCl溶液后,滴加 KI 溶液 | 先产生白色沉淀,后出现黄色沉淀 | 证明Ksp(AgI)<Ksp(AgCl) |
A.AB.BC.CD.D