题目内容
A、B、C、D、E、F均为短周期元素,且原子序数依次增大,A是原子半径最小的元素,B的最髙价氧化物的水化物可与其氢化物反应形成离子化合物甲;A与D可以按照原子个数比4 : 1形成化合物乙,且乙分子中含有18个电子,E与B同主族,C的阳离子与F的阴离子相差一个电子层,且可形成离子个数比为
2 : 1的离子化合物丙。
(1) D的原子结构示意图为 (1分),丙的电子式为 (2分),E在周期表中的位置为 (2分)。
(2) 下列说法正确的有 (2分)。
①化合物乙为正四面体形分子,是由极性键构成的非极性分子
②C、D、E、F原子半径由大到小的顺序为C>D>E>F
③B、E形成的氢化物中,B的氢化物稳定性更强,是因为该分子中存在氢键
④化合物甲和化合物丙都含有离子键和共价键
(3) 已知通常状况下1gF在空气中完全燃烧放出a kj的热量,请写出表示F燃烧热的热化学方程式 (2分)。将燃烧产物通入BaCl2和HNO3的混合溶液,生成白色沉淀并放出无色气体,请用一个离子方程式表示该反应 (2 分)。
(4) 写出一个由以上元素构成的1Oe-微粒与18e-微粒反应的离子方程式:
(2分)及其他合理答案。
2 : 1的离子化合物丙。
(1) D的原子结构示意图为 (1分),丙的电子式为 (2分),E在周期表中的位置为 (2分)。
(2) 下列说法正确的有 (2分)。
①化合物乙为正四面体形分子,是由极性键构成的非极性分子
②C、D、E、F原子半径由大到小的顺序为C>D>E>F
③B、E形成的氢化物中,B的氢化物稳定性更强,是因为该分子中存在氢键
④化合物甲和化合物丙都含有离子键和共价键
(3) 已知通常状况下1gF在空气中完全燃烧放出a kj的热量,请写出表示F燃烧热的热化学方程式 (2分)。将燃烧产物通入BaCl2和HNO3的混合溶液,生成白色沉淀并放出无色气体,请用一个离子方程式表示该反应 (2 分)。
(4) 写出一个由以上元素构成的1Oe-微粒与18e-微粒反应的离子方程式:
(2分)及其他合理答案。
(1) 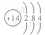 (1分),
(1分),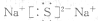 (2分),第三周期V A族(2分)。
(2分),第三周期V A族(2分)。
(2)①②(2分)。
(3)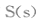
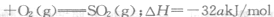 (2分)。
(2分)。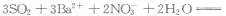
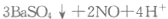 (2 分)。
(2 分)。
(4)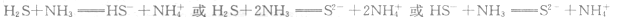
(2分)
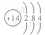 (1分),
(1分),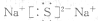 (2分),第三周期V A族(2分)。
(2分),第三周期V A族(2分)。(2)①②(2分)。
(3)
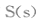
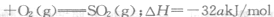 (2分)。
(2分)。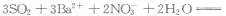
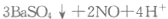 (2 分)。
(2 分)。(4)
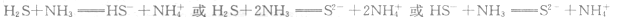
(2分)
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
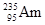 ,它和铀
,它和铀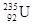 比较,下列叙述中正确的是
比较,下列叙述中正确的是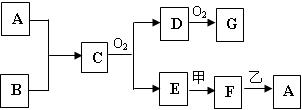
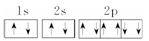

 的原子半径随元素原子序数的递增呈周期性变化
的原子半径随元素原子序数的递增呈周期性变化