题目内容
【题目】H2S废气资源化的原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l) ΔH =-632 kJ·mol-1。下图为H2S燃料电池的示意图。下列说法正确的是
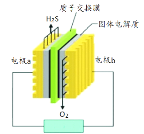
A. 电极b为电池的负极
B. 电极b上发生的电极反应为:O2 + 2H2O + 4e- = 4OH-
C. 电路中每流过4 mol电子,电池会产生632 kJ电能
D. 每34 g H2S参与反应,有2 molH+经质子膜进入正极区
【答案】D
【解析】
燃料电池属于原电池,应根据原电池原理分析回答。
图中,H2S在电极a上失电子,a是负极;O2在电极b上得电子,b是正极(A项错误)。电池使用质子(H+)交换膜,说明固体电解质呈酸性,则负极反应为2H2S-4e-=S2+4H+,正极反应为O2 + 4e- +4H+ = 2H2O(B项错误)。据热化学方程式,电路中转移4 mol电子,共放出热量632 kJ(包括电能、热量等),故电能小于632 kJ(C项错误)。由电极反应式知,每1molH2S(34g)参与反应,有2 mol H+经质子膜进入正极区,才能使两极电解质呈电中性(D项正确)。
本题选D。

【题目】(1)反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)![]() FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1、K2的值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1、K2的值如下表:
700 ℃ | 900 ℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
①反应CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH的平衡常数为K,则ΔH=________(用ΔH1和ΔH2表示),K=________(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)
CO(g)+H2O(g) ΔH的平衡常数为K,则ΔH=________(用ΔH1和ΔH2表示),K=________(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)![]() CO(g)+H2O(g)是_____________________反应(填“吸热”或“放热”)。
CO(g)+H2O(g)是_____________________反应(填“吸热”或“放热”)。
②能判断CO2(g)+H2(g)![]() CO(g)+H2O(g)达到化学平衡状态的依据是_______(填字母)。
CO(g)+H2O(g)达到化学平衡状态的依据是_______(填字母)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO)=c(CO2)
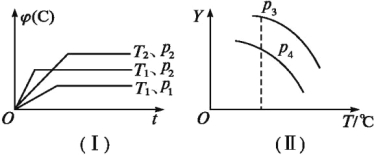
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
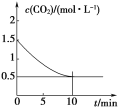
①该条件下反应的平衡常数为______;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为______mol·L-1。
②下列措施中能使平衡时 增大的是________(填字母)。
增大的是________(填字母)。
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉