题目内容
10.如图装置或操作能达到实验目的是( )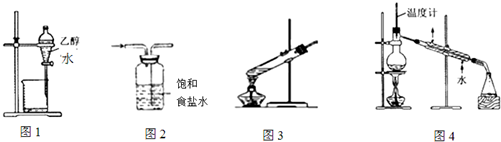
| A. | 图1装置用于分离乙醇和水 | B. | 图2装置用于除去氯气中的氯化氢 | ||
| C. | 图3装置用于葡萄糖的银镜反应 | D. | 图4装置用于石油的蒸馏 |
分析 A.乙醇与水互溶,不能用分液方法分离;
B.气流方向为“长进短出”;
C.银镜反应应采取水浴加热;
D.蒸馏操作过程中,温度计应该放在蒸馏烧瓶的支管口处,冷凝管采用的是逆向通水法.
解答 解:A.分离互不相溶的液体采取分液方法,乙醇与水互溶,不能用分液方法分离,故A错误;
B.气流方向为“长进短出”,若“短进长出”,气压增大会将饱和食盐水压出,故B错误;
C.银镜反应应采取水浴加热,直接加热可能为发生爆炸危险,故C错误;
D.蒸馏操作过程中,温度计应该放在蒸馏烧瓶的支管口处,冷凝管采用的是逆向通水法,这样使水能够与冷凝管中物质充分接触,冷凝效果好,故D正确,
故选D.
点评 本题考查学生对实验装置的理解、分析与评价,是对实验基础的综合考查,难度不大.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
1.2010年8月15日为舟曲特大山洪泥石流灾害全国哀悼日,为防止大灾之后有大疫,灾区的饮用水消毒是防止病从口入的措施之一.高铁酸钠是一种新型、高效、多功能水处理剂,高铁酸钠(Na2FeO4)制备方法有:
湿法制备的主要反应为:2Fe(OH)3+3ClO-+4OH-═2FeO42-+3Cl-+5H2O,
干法制备的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法不正确的是( )
湿法制备的主要反应为:2Fe(OH)3+3ClO-+4OH-═2FeO42-+3Cl-+5H2O,
干法制备的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法不正确的是( )
| A. | 高铁酸钠中铁显+6价 | |
| B. | 湿法中每生成1 mol Na2FeO4转移3 mol电子 | |
| C. | 干法中每生成1 mol Na2FeO4转移3 mol电子 | |
| D. | Na2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3还能吸附水中的悬浮杂质 |
18.下列推断正确的是( )
| A. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| B. | SiO2 是酸性氧化物,能与NaOH溶液反应 | |
| C. | Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 | |
| D. | SO2和新制氯水均有漂白性,将SO2和Cl2通入滴加少量紫色石蕊试液,充分振荡后溶液最终呈无色 |
5.m g 铜与足量浓硫酸完全反应,放出的气体经干燥后为n L,则被还原的硫酸为( )
| A. | $\frac{m}{64}$ g | B. | $\frac{48m}{32}$$\frac{49m}{32}$g | C. | $\frac{n}{22.4}$mol | D. | 不能确定 |
15.为扩大现有资源的使用效率,在一些油品中加入了降凝制剂J,以降低油料的凝固点,扩大燃料油的使用范围.J是一种高分子化合物: 下列有关J的说法正确的是( )
下列有关J的说法正确的是( )
 下列有关J的说法正确的是( )
下列有关J的说法正确的是( )| A. | J是由2种单体缩聚而成的 | B. | J是由2种单体加聚而成的 | ||
| C. | J具有可燃性 | D. | J没有可燃性 |
2.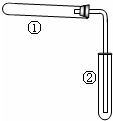 如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
 如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )| ①中实验 | ②中现象 |
| 铁粉与水蒸气加热 | 肥皂水冒泡 |
| 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
| NaHCO3 | 澄清石灰水变浑浊 |
| 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
19.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1molCH3+(碳正离子)中含有电子数为10NA | |
| B. | 1mol铜与足量硫蒸气反应,转移电子数为2NA | |
| C. | 用惰性电极电解CuCl2溶液,阴极析出32g铜时,线路中通过的电子数为NA | |
| D. | 0.84g NaHCO3晶体中阳离子和阴离子总数为0.03NA |
2.下列关于无机非金属材料的说法中正确的是( )
| A. | 传统无机非金属材料是指:光导纤维、玻璃、水泥、陶瓷等硅酸盐材料 | |
| B. | 新型无机非金属材料虽然克服了传统无机非金属材料的缺点,但强度比较差 | |
| C. | 高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点 | |
| D. | 传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐 |

 .
. .
.