题目内容
2.物质之间发生化反应时,一定发生变化的是( )| A. | 颜色 | B. | 状态 | C. | 能量 | D. | 原子核 |
分析 化学反应的实质是原子的重新组合,旧键的断裂和新键的形成,旧键断裂吸收能量,新键形成释放能量,与颜色和状态无必然联系.
解答 解:A.H2和Cl2发生反应,物质的颜色发生变化,HCl(aq)和NaOH(aq)发生反应,物质的颜色没有发生变化,故A错误;
B.H2和Cl2反应,物质的状态没有发生变化--反应前后都是气体,H2和O2发生反应,恢复到原来的温度,物质的状态发生了变化,故B错误;
C.化学反应的实质又是旧键的断裂和新键的形成,旧键断裂吸收能量,新键形成释放能量,一定有能量变化,故C正确;
D.化学反应的实质是原子的重新组合,原子核没有发生变化,故D错误.
故选C.
点评 本题考查化学反应的主要特点,题目难度不大,学习中注意相关基础知识的积累.

练习册系列答案
相关题目
13.将几种铁的氧化物的混合物加入100mL、7mol•L-1的盐酸中.氧化物恰好完全溶解,在所得的溶液中通入0.56L(标准状况)氯气时,恰好使溶液中的Fe2+完全转化为Fe3+,则该混合物中铁元素的质量分数为( )
| A. | 72.4% | B. | 71.4% | C. | 79.0% | D. | 63.6% |
10.下表是元素周期表的一部分.表中所列的字母分别代表某一化学元素.
请用具体的元素符号填写下面空格:
(1)以上元素中,第一电离能最大的是Ar;电负性最大的金属是O.
(2)i、j、l 三种元素最高价氧化物对应的水化物中,酸性最强的是HClO4
(3)根据元素原子的外围电子排布的特征,可将元素周期表分成几个区域,其中,元素c、m分别位于ds区、p区.
(4)下表是一些气态基态原子的第一、二、三、四级电离能(kJ•mol-1):
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量Li原子失去1个电子后形成稳定结构,再失去1个电子很困难
②表中X可能为以上元素中的Al元素.用元素符号表示a和h形成化合物的电子式是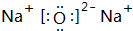 和
和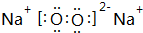 .
.
| b | |||||||||||||||||
| h | |||||||||||||||||
| a | f | i | j | l | m | ||||||||||||
| e | c | g | |||||||||||||||
(1)以上元素中,第一电离能最大的是Ar;电负性最大的金属是O.
(2)i、j、l 三种元素最高价氧化物对应的水化物中,酸性最强的是HClO4
(3)根据元素原子的外围电子排布的特征,可将元素周期表分成几个区域,其中,元素c、m分别位于ds区、p区.
(4)下表是一些气态基态原子的第一、二、三、四级电离能(kJ•mol-1):
| 锂 | X | |
| 第一电离能 | 519 | 580 |
| 第二电离能 | 7296 | 1820 |
| 第三电离能 | 11799 | 2750 |
| 第四电离能 | 11600 |
②表中X可能为以上元素中的Al元素.用元素符号表示a和h形成化合物的电子式是
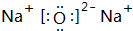 和
和 .
.
7.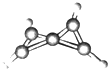 科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是( )
科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是( )
 科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是( )
科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是( )| A. | 烃X的分子式为C5H4 | |
| B. | 分子中只有一种类型的H原子 | |
| C. | 烃X在一定条件下能发生加成反应 | |
| D. | X分子中只有碳碳单键,没有碳碳双键 |
14.下列粒子半径最大的是( )
| A. | Na+ | B. | P | C. | Cl | D. | F |
11.下列有关氯气的说法正确的是( )
| A. | 氯气是黄绿色气体,有毒,有刺激性气味,不能溶于水 | |
| B. | 将氯气持续通入紫色石蕊试液中,现象是石蕊试液先变红后褪色 | |
| C. | 红热的铜丝在Cl2 中燃烧产生棕黄色的雾;H2 在Cl2 中燃烧,火焰呈淡蓝色 | |
| D. | 氯水长时间放置不会变质,还可消毒杀菌 |
12.下列各组中互为同位素的一组是( )
| A. | O2、O3 | B. | Na2O、Na2O2 | C. | 40K、40Ca | D. | H、D、T |