题目内容
1.下列措施对增大反应速率明显有效的是( )| A. | Na与水反应时增大水的用量 | |
| B. | CaCO3与盐酸反应制取CO2时,改用浓硫酸 | |
| C. | C(s)+H2O(g)?CO(g)+H2(g),将碳块改成碳粉进行实验 | |
| D. | 粗锌与盐酸反应,将粗锌换成纯锌 |
分析 A、钠与水反应剧烈,加水不能改变浓度;
B、浓硫酸与碳酸钙反应生成微溶的硫酸钙阻止反应进一步进行;
C、将碳块改成碳粉进行实验,增大了固体接触面积;
D、粗锌里含有杂质金属与酸反应时可形成原电池装置,而纯锌不能形成原电池装置.
解答 解:A、加水不能改变浓度水的浓度,对反应速率没有影响,故A错误;
B、浓硫酸与碳酸钙反应生成微溶的硫酸钙阻止反应进一步进行,所以不能提高生成气体的反应速率,故B错误;
C、将碳块改成碳粉进行实验,增大了固体接触面积,反应速率增大,故C正确;
D、粗锌里含有杂质金属与酸反应时可形成原电池装置,而纯锌不能形成原电池装置,所以将粗锌换成纯锌,反应速率减慢,故D错误;
故选:C.
点评 本题考查化学反应速率的影响因素,题目难度不大,注意基础知识的积累.

练习册系列答案
相关题目
11.反应下列原子或离子核外电子未成对电子数最多的是( )
| A. | N | B. | Ni | C. | Cr | D. | Cu+ |
12.航天飞船可用肼(电子式为 )作动力源.已知1g液态肼和足量的液态过氧化氢(结构式为H-O-O-H)反应生成N2和水蒸气时放出20.05kJ热量,化学方程式如下:N2H4+2H2O2═N2↑+4H2O.下列说法中错误的是( )
)作动力源.已知1g液态肼和足量的液态过氧化氢(结构式为H-O-O-H)反应生成N2和水蒸气时放出20.05kJ热量,化学方程式如下:N2H4+2H2O2═N2↑+4H2O.下列说法中错误的是( )
 )作动力源.已知1g液态肼和足量的液态过氧化氢(结构式为H-O-O-H)反应生成N2和水蒸气时放出20.05kJ热量,化学方程式如下:N2H4+2H2O2═N2↑+4H2O.下列说法中错误的是( )
)作动力源.已知1g液态肼和足量的液态过氧化氢(结构式为H-O-O-H)反应生成N2和水蒸气时放出20.05kJ热量,化学方程式如下:N2H4+2H2O2═N2↑+4H2O.下列说法中错误的是( )| A. | 该动力源的突出优点之一是反应产物对环境无污染 | |
| B. | 液态肼燃烧生成1 mol N2时放出的热量为20.05 kJ | |
| C. | 该反应中肼作氧化剂 | |
| D. | 肼和过氧化氢中的化学键类型相同 |
9.下列有关化学用语使用正确的是( )
| A. | 乙烯的结构式为:CH2CH2 | |
| B. | NH4C1的电子式: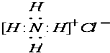 | |
| C. | Cr原子 的基态简化电子排布式为[Ar]3d54s1 | |
| D. | S原子的价电子轨道表示式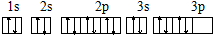 |
13.分子式为C6H12O2,属于乙酸乙酯同系物的同分异构体共有( )
| A. | 12种 | B. | 16种 | C. | 20种 | D. | 24种 |
10.北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,有良好的超导性.下列关于K3C60的组成和结构分析正确的是( )
| A. | K3C60中既有离子键,又有共价键 | |
| B. | 1molK3C60中含有的离子数目为63×6.02×1023 | |
| C. | 通常条件下该晶体有良好的导电性 | |
| D. | 该物质的化学式可写为KC20 |
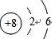 .
.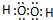 ,化合物XYZ的结构式
,化合物XYZ的结构式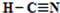 .
.