题目内容
9.下列由相关实验现象所推出的结论正确的是( )| A. | Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 | |
| B. | HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 | |
| C. | Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 | |
| D. | 分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
分析 A.二氧化硫与品红化合生成无色物质;
B.由阳离子、阴离子离子构成的化合物化合物是离子化合物,一般由活泼金属和活泼非金属元素组成;
C.Fe与稀HNO3反应生成NO;
D.HCl、NH3均极易溶于水.
解答 解:A.二氧化硫与品红化合生成无色物质,体现其漂白性,而Cl2能使品红溶液褪色,说明其氧化性,故A错误;
B.氯化氢是共价化合物,故B错误;
C.Fe与稀HNO3反应生成NO,该反应不是置换反应,Fe与稀H2SO4反应有氢气生成,属于置换反应,故C错误;
D.HCl、NH3均极易溶于水,则分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,故D正确.
故选D.
点评 本题考查物质的性质,为高频考点,综合考查元素化合物知识,把握物质的性质及发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
19.下列相关实验不能达到预期目的是( )
| 相关实验 | 预期目的 | |
| ① | 在两份同浓度同体积的H2O2溶液中,分别加2滴FeCl3溶液和2滴CuCl2溶液,前者放在热水中,后者放在冰水中.观察气泡快慢; | 验证温度对化学反应速率的影响. |
| ② | 将氯水加入淀粉KI溶液中 | 验证Cl的非金属性比I强 |
| ③ | 在相同温度下,将表面积相同的铝条和镁条投入等体积同浓度的盐酸中,观察产生气泡的速率. | 比较同周期金属元素的金属性强弱. |
| ④ | 利用电解质溶液的导电性装置,检测AlCl3溶液的导电性 | 证明AlCl3是离子化合物 |
| A. | 仅① | B. | ①④ | C. | ②③ | D. | ③④ |
14.下列除去杂质的方法正确的是( )
| A. | KNO3溶液中混有少量K2SO4,加入适量BaCl2溶液 | |
| B. | 二氧化碳气体中混有少量二氧化硫:通入酸性高锰酸钾溶液,收集气体 | |
| C. | 除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 | |
| D. | 除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
1.下列变化中,一定不存在化学能与热能相互转化的是( )
| A. | 铁丝燃烧 | B. | 白磷自燃 | C. | 燃放爆竹 | D. | 干冰气化 |
11.阿司匹林( 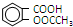 )是世界上应用最广泛的解热、镇痛药.因乙酸很难与酚羟基酯化,工业上以水杨酸(
)是世界上应用最广泛的解热、镇痛药.因乙酸很难与酚羟基酯化,工业上以水杨酸( 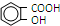 )与乙酸酐[(CH3CO)2O]为主要原料合成阿司匹林.粗产品中主要的副产物是水杨酸多聚物,需进一步提纯.反应原理和相关物理数据如下:
)与乙酸酐[(CH3CO)2O]为主要原料合成阿司匹林.粗产品中主要的副产物是水杨酸多聚物,需进一步提纯.反应原理和相关物理数据如下:
 +(CH3CO)2O$?_{△}^{浓硫酸}$
+(CH3CO)2O$?_{△}^{浓硫酸}$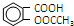 +CH3COOH
+CH3COOH
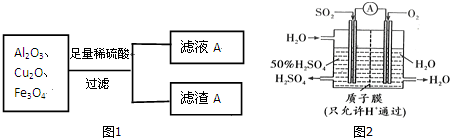
如图1是工业上制备并提纯阿司匹林的部分流程:
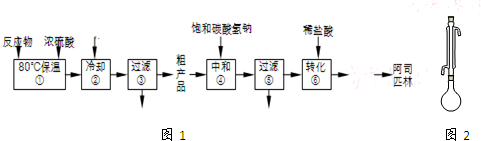
完成下列填空:
(1)步骤①的反应装置如图2所示(加热装置未画出),实验仪器必须干燥的原因是防止乙酸酐与水反应生成乙酸,不利于反应发生;冷凝管的作用是冷凝回流;对烧瓶进行加热的合适方法是水浴加热.
(2)反应中加入的乙酸酐是过量的,过量的目的是提高水杨酸的转化率;步骤②中加入水的目的是使乙酸酐转化为乙酸,同时放出大量的热,需冷却至常温再进行过滤,冷却的目的是减少阿司匹林因溶解而损失(使阿司匹林结晶析出);检验步骤③所得滤液中是否含有水杨酸,可选用的试剂是FeCl3.(写化学式)
(3)步骤④中加入NaHCO3的目的是使阿司匹林转化为易溶于水的盐.
(4)步骤⑤过滤得到的滤渣主要是水杨酸多聚物.步骤⑥中加入盐酸后发生反应的化学方程式为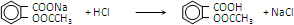 .
.
(5)从步骤⑥到成品纯阿司匹林的剩余操作依次有结晶、过滤、洗涤、干燥.
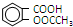 )是世界上应用最广泛的解热、镇痛药.因乙酸很难与酚羟基酯化,工业上以水杨酸(
)是世界上应用最广泛的解热、镇痛药.因乙酸很难与酚羟基酯化,工业上以水杨酸( 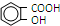 )与乙酸酐[(CH3CO)2O]为主要原料合成阿司匹林.粗产品中主要的副产物是水杨酸多聚物,需进一步提纯.反应原理和相关物理数据如下:
)与乙酸酐[(CH3CO)2O]为主要原料合成阿司匹林.粗产品中主要的副产物是水杨酸多聚物,需进一步提纯.反应原理和相关物理数据如下: +(CH3CO)2O$?_{△}^{浓硫酸}$
+(CH3CO)2O$?_{△}^{浓硫酸}$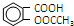 +CH3COOH
+CH3COOH| 名称 | 常温下状态 | 水中溶解性 |
| 乙酸酐 | 液 | 与水反应 |
| 阿司匹林 | 固 | 冷水中微溶;热水中易溶 |
| 水杨酸多聚物 | 固 | 难溶 |

完成下列填空:
(1)步骤①的反应装置如图2所示(加热装置未画出),实验仪器必须干燥的原因是防止乙酸酐与水反应生成乙酸,不利于反应发生;冷凝管的作用是冷凝回流;对烧瓶进行加热的合适方法是水浴加热.
(2)反应中加入的乙酸酐是过量的,过量的目的是提高水杨酸的转化率;步骤②中加入水的目的是使乙酸酐转化为乙酸,同时放出大量的热,需冷却至常温再进行过滤,冷却的目的是减少阿司匹林因溶解而损失(使阿司匹林结晶析出);检验步骤③所得滤液中是否含有水杨酸,可选用的试剂是FeCl3.(写化学式)
(3)步骤④中加入NaHCO3的目的是使阿司匹林转化为易溶于水的盐.
(4)步骤⑤过滤得到的滤渣主要是水杨酸多聚物.步骤⑥中加入盐酸后发生反应的化学方程式为
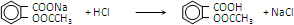 .
.(5)从步骤⑥到成品纯阿司匹林的剩余操作依次有结晶、过滤、洗涤、干燥.
12.某些芳香族化合物与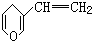 互为同分异构体,其中与FeCl3溶液混合后显色和不显色的种类分别有( )
互为同分异构体,其中与FeCl3溶液混合后显色和不显色的种类分别有( )
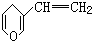 互为同分异构体,其中与FeCl3溶液混合后显色和不显色的种类分别有( )
互为同分异构体,其中与FeCl3溶液混合后显色和不显色的种类分别有( )| A. | 2种和1种 | B. | 2种和3种 | C. | 3种和2种 | D. | 3种和1种 |

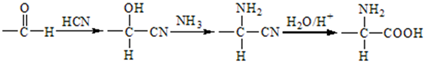
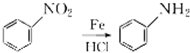
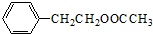 +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$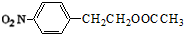 +H2O.
+H2O.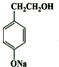 .
.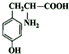 .
.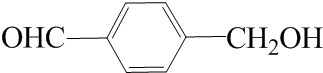 (写结构简式).
(写结构简式).