题目内容
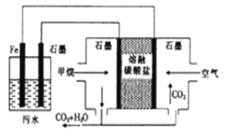
【题目】烟气中主要污染物为SO2、NO、NO2,可用如图工艺进行脱硫脱硝及产物回收。
(1)空气预处理过程中,发生主要反应的化学方程式为_______。
(2)洗气过程中,尿素作还原剂,转化成两种无污染的气体的化学式是_______
(3)充分曝气氧化过程中,发生反应的含镁化合物是_________。
(4)完成沉镁过程中生成碱式碳酸镁的离子方程式___Mg2++____= MgCO3Mg(OH)2↓+__CO2↑+____H2O
(5)(NH4)2SO4粗品中含有的主要杂质为_________(填名称)。
(6)碱式碳酸镁经过简单加工可循环利用,加工过程发生反应的化学方程式为______。
【答案】2NO + O2 = 2NO2 CO2、N2 MgSO3 2 4HCO3- 3 1 硝酸铵 MgCO3·Mg(OH)2![]() 2MgO+CO2↑+H2O
2MgO+CO2↑+H2O
【解析】
根据题中工业流程可知,烟气中主要污染物为SO2、NO、NO2,在空气中预处理时,主要将NO氧化成NO2,再用含尿素的氧化镁悬浊液还原生成氮气和二氧化碳,同时溶液中有硫酸镁、亚硫酸镁、硝酸镁等物质生成,在充分曝气氧化中,亚硫酸镁被氧化成硫酸镁,再加入碳酸氢铵溶液生成碱式碳酸镁沉淀,过滤后将滤液浓缩结晶可得硫酸铵晶体。
(1)在空气中预处理时,主要将NO氧化成NO2,发生主要反应的化学方程式为2NO+O2=2NO2;
(2)根据上面的分析可知,洗气过程中,生成两种无污染的气体是CO2、N2,
(3)在充分曝气氧化中,亚硫酸镁被氧化成硫酸镁,发生反应的为MgSO3;
(4)镁离子和碳酸氢根离子发生双水解,生成碱式碳酸镁,根据电荷守恒和元素守恒可知其离子反应方程式为2Mg2++4HCO3-=MgCO3·Mg(OH)2↓+3CO2↑+H2O;
(5)根据物料守恒,在Mg2+和HCO3-发生反应生成碱式碳酸镁时,还有硫酸铵、硝酸铵生成,因此(NH4)2SO4粗品中含有的主要杂质为硝酸铵;
(6) 碱式碳酸镁经过加热生成氧化镁和二氧化碳及水,氧化镁可循环利用,反应的方程式为MgCO3·Mg(OH)2![]() 2MgO+CO2↑+H2O。
2MgO+CO2↑+H2O。

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案