题目内容
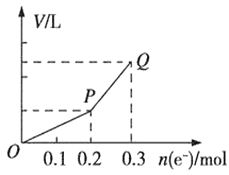
【题目】用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。Q点时欲使溶液恢复到起始状态,可向溶液中加入
A. 0.1 mol CuO
B. 0.1 mol CuCO3
C. 0.1 mol Cu(OH)2
D. 0.05 mol Cu2(OH)2CO3
【答案】D
【解析】
试题用惰性电极电解硫酸铜溶液时,先发生反应2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4,当铜离子完全析出时,发生反应2H2O
2Cu+O2↑+2H2SO4,当铜离子完全析出时,发生反应2H2O![]() 2H2↑+O2↑,根据图象知,转移电子0.2mol时只有气体氧气生成,发生反应2CuSO4+2H2O
2H2↑+O2↑,根据图象知,转移电子0.2mol时只有气体氧气生成,发生反应2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4,实际上相当于析出氧化铜,根据氧化铜和转移电子之间的关系式得n(Cu)=0.2mol/2=0.1mol,所以相当于析出0.1molCuO;继续电解发生的反应为2H2O
2Cu+O2↑+2H2SO4,实际上相当于析出氧化铜,根据氧化铜和转移电子之间的关系式得n(Cu)=0.2mol/2=0.1mol,所以相当于析出0.1molCuO;继续电解发生的反应为2H2O![]() 2H2↑+O2↑,实际上是电解水,根据水和转移电子之间的关系式得m(H2O)=(0.3-0.2)/4mol=0.25mol,所以电解水的质量是0.25mol,根据“析出什么加入什么”的原则知,要使溶液恢复原状,应该加入0.1mol氧化铜和0.05mol水;A.只加氧化铜不加水不能使溶液恢复原状,故A错误;B.加入碳酸铜时,碳酸铜和稀硫酸反应生成硫酸铜和二氧化碳,所以相当于加入氧化铜,没有加入水,所以不能使溶液恢复原状,故B错误;C.0.075mol Cu(OH)2相当于加入0.075molCuO和0.075molH2O,与析出物质的物质的量不同,所以不能恢复原状,故C错误;D.0.05mol Cu2(OH)2CO3,碱式碳酸铜和硫酸反应生成硫酸铜、水和二氧化碳,根据原子守恒知,相当于加入0.1molCuO和0.05mol的水,所以能使溶液恢复原状,故D正确;答案为D。
2H2↑+O2↑,实际上是电解水,根据水和转移电子之间的关系式得m(H2O)=(0.3-0.2)/4mol=0.25mol,所以电解水的质量是0.25mol,根据“析出什么加入什么”的原则知,要使溶液恢复原状,应该加入0.1mol氧化铜和0.05mol水;A.只加氧化铜不加水不能使溶液恢复原状,故A错误;B.加入碳酸铜时,碳酸铜和稀硫酸反应生成硫酸铜和二氧化碳,所以相当于加入氧化铜,没有加入水,所以不能使溶液恢复原状,故B错误;C.0.075mol Cu(OH)2相当于加入0.075molCuO和0.075molH2O,与析出物质的物质的量不同,所以不能恢复原状,故C错误;D.0.05mol Cu2(OH)2CO3,碱式碳酸铜和硫酸反应生成硫酸铜、水和二氧化碳,根据原子守恒知,相当于加入0.1molCuO和0.05mol的水,所以能使溶液恢复原状,故D正确;答案为D。

 名校课堂系列答案
名校课堂系列答案【题目】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
I1 | I2 | I3 | I4 | I5 | |
电离能 | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是_________价,其基态原子电子排布式为_________。
(2)Ca3(PO4)3F中非金属元素电负性由大到小的顺序为_________。
(3)PO43-的中心原子的杂化方式为_________,该离子的空间构型为_________,键角为________,其等电子体有_________ (请写出两种)。
(4)CaF2晶胞结构如图所示,则CaF2晶体中与Ca2+最近且等距离的Ca2+数目为_________;已知Ca2+和F半径分别为a cm、b cm,阿伏加德罗常数为NA,M为摩尔质量,则晶体密度为________g·cm3(不必化简)。
(5)已知MgO与CaO的晶体结构相似,其摩氏硬度的大小关系为_________,原因为___________。