题目内容
18.物质的量浓度相同的下列各溶液,由水电离出的c(H+)由大到小的顺序是( )①NaHSO4 ②NaHCO3 ③Na2CO3 ④Na2SO4.
| A. | ④③②① | B. | ①②③④ | C. | ③②④① | D. | ③④②① |
分析 根据酸对水的电离起抑制作用,能水解的盐对水的电离起到促进作用,不水解的盐对水的电离无影响,水的电力程度越大,电离出的氢离子或是氢氧根离子浓度越大.
解答 解:A、NaHSO4是强电解质,能完全电离出氢离子,显示强酸性,对水的电离抑制程度最大,故由水电离出的氢氧根浓度最小;
NaHCO3和Na2CO3都是能水解的盐,对水的电离起到促进的作用,碳酸钠中碳酸根的水解程度大于碳酸氢钠中碳酸氢根离子的水解程度,所以碳酸钠对水的电离起到的促进作用大,由水电离出的氢氧根浓度是碳酸钠大于碳酸氢钠,硫酸钠不水解,对水的电离程度无影响,
综上由水电离出的氢氧根浓度由大到小的顺序是③②④①,
故选C.
点评 本题考查学生有关水的电离平衡的影响知识,掌握酸和碱抑制水的电离,而盐的水解促进水的电离,盐的水解程度越大,对水的电离的促进程度越大,难度不大.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
9.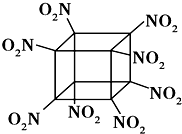 科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )
科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )
 科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )
科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )| A. | 分子中C、N间形成非极性键 | |
| B. | 1mol该分子中含8mol二氧化氮 | |
| C. | 该物质可能由立方烷发生取代反应而得 | |
| D. | 该物质爆炸产物是NO2、C02、H20 |
6.欲使NaCl、NH4Cl和SiO2的混合物分开,其必要的操作为( )
| A. | 升华、溶解、过滤、蒸发 | B. | 溶解、过滤、蒸发、分液 | ||
| C. | 加热、溶解、过滤、结晶 | D. | 溶解、过滤、分馏、结晶 |
3.下列说法正确的是( )
| A. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃的条件下△H应该不相同 | |
| B. | 化学反应中的能量变化都表现为热量变化 | |
| C. | 任何放热反应在常温下一定能发生 | |
| D. | 反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
10.关于胶体,下列说法正确的是( )
| A. | 胶体的聚沉是化学变化 | |
| B. | 含有0.01mol FeCl3的溶液制成的胶体中,胶体粒子的数目约为6.02×1021个 | |
| C. | 胶体的介稳性与胶体带有电荷有关 | |
| D. | NaCl晶体既可制成溶液又可制成胶体 |
7.下列有机化合物的性质能体现是羟基对苯环产生影响的是( )
| A. | 苯酚溶液显弱酸性 | |
| B. | 苯酚和乙醇中,分别加入金属钠,苯酚反应剧烈 | |
| C. | 苯酚比苯容易发生溴代反应 | |
| D. | 苯酚能与氢氧化钠溶液反应,而苯甲醇不能 |