题目内容
25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2 800 kJ/mol,则下列热化学方程式正确的是( )
A.C(s)+ O2(g)=CO(g);△H=-393.5 kJ/mol
B.2H2(g)+O2(g)=2H2O(g);△H=+571.6 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-890.3 kJ/mol
D.C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1 400 kJ/mol
D
解析:
本题主要考查对燃烧热概念的理解和对热化学方程式的掌握情况。
燃烧热是1mol可燃物完全燃烧生成稳定氧化物和液态水时的反应热。而判断一个热化学方程式的正误通常要检查它的物质聚集状态、化学计量数、反应热的数值符号等。A中碳完全燃烧时生成的稳定氧化物应该是二氧化碳而不是一氧化碳,A不正确;B中氢气燃烧是一个放热反应,△H的不可能是一个正数,B不正确;热化学方程式C中的反应热是甲烷的燃烧热,但是生成的水是气态,所以C也不正确。

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列有关热化学方程式的评价合理的是( )
|
25℃、101kPa下:
①2Na(s)+
O2(g)═Na2O(s)△H1=-414kJ/mol;
②2Na(s)+O2(g)═Na2O2(s)△H2=-511kJ/mol.
下列说法正确的是( )
①2Na(s)+
| 1 |
| 2 |
②2Na(s)+O2(g)═Na2O2(s)△H2=-511kJ/mol.
下列说法正确的是( )
| A、①和②生成等物质的量的产物,转移的电子数相同 |
| B、Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| C、25℃、101 kPa下,Na2O2(s)+2Na(s)═2Na2O(s)△H=+317 kJ/mol |
| D、①和②产物中的阴阳离子个数比均为1:1 |
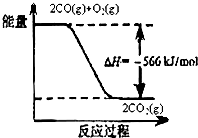 已知:
已知: