题目内容
11.将标准状况下的2mol O2和8mol N2混合,求混合气体的平均相对分子质量.分析 根据M=$\frac{m}{n}$计算,摩尔质量在数值上等于相对分子质量.
解答 解:标准状况下的2mol O2和8mol N2混合,气体的总质量为2mol×32g/mol+8mol×28g/mol=288g,
则混合气体的平均摩尔质量为$\frac{288g}{10mol}$=28.8g/mol,
所以混合气体的平均相对分子质量为28.8.
答:混合气体的平均相对分子质量为28.8.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握相关计算公式,难度不大.

练习册系列答案
相关题目
1.下列叙述中正确的是( )
| A. | 第三周期元素的离子半径从左到右依次减小 | |
| B. | HCl、PCl5、N2、CO2分子中所有原子都满足最外层8电子的结构 | |
| C. | 晶体内可以不存在化学键,也可以同时存在离子键和共价键 | |
| D. | 若某离子化合物X2Y3中X3+和Y2-的电子层结构相同,则X、Y两元素的原子序数之差可能是5、15或29 |
16.用NA表示阿伏加德罗常数的值,1.5mol HCl气体中所含原子的数目是( )
| A. | NA | B. | 2NA | C. | 3NA | D. | 4NA |
3.在一定温度下的定容密闭容器中,取一定的A,B于反应容器中,当下列物理量不再改变时,表明反应:A(s)+2B(g)?C(g)+D(g)已达平衡状态的是( )
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | C、D的物质的量的比值 | D. | 气体的总物质的量 | ||
| E. | 气体的平均摩尔质量 |
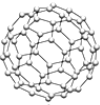 氢气作为一种清洁能源,必须解决它的储存问题,C60(结构见图)可用作储氢材料,已知C60中每个碳原子均达到8电子稳定结构.
氢气作为一种清洁能源,必须解决它的储存问题,C60(结构见图)可用作储氢材料,已知C60中每个碳原子均达到8电子稳定结构.