题目内容
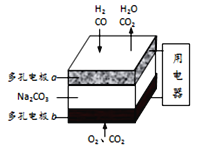
【题目】以熔融Na2CO3为电解质,H2和CO混合气为燃料的电池原理如图所示。下列说法正确的是( )
A. b是电池的负极
B. 该电池使用过程中需补充Na2CO3
C. a、b两级消耗气体的物质的量之比为2:1
D. 电极a上每消耗22.4L原料气体,电池中转移电子数约为2NA
【答案】C
【解析】b电极上为氧气得电子与二氧化碳反应生成CO32-,则b是电池的正极,故A错误; 电池总反应是氢气与氧气生成水、CO与氧气反应生成二氧化碳,该电池使用过程中不消耗碳酸钠,所以不需要补充Na2CO3,故B错误;电极a反应为:CO+CO32ˉ-2eˉ═2CO2,H2+CO32ˉ-2eˉ═H2O+CO2,b极反应为O2+2CO2+4e-=2CO32-,则a、b两极消耗的气体的物质的量之比是2:1,故C正确. D.未指明标准状况,无法计算,故D错误;

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目