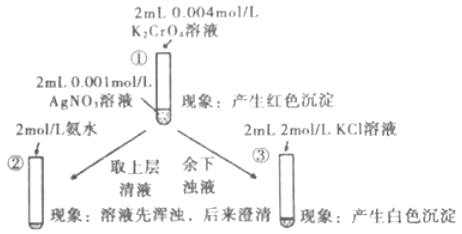
题目内容
【题目】炼油厂烷基化反应产生的废液中含硫酸91%、难挥发有机物7%。实验室以软锰矿(主要含MnO2,还含少量Fe、Al等元素)处理废液并制取MnSO4·H2O晶体,其实验流程如图:
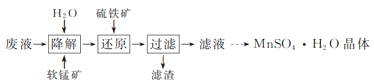
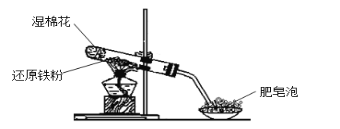
(1)研究温度对“降解”过程中有机物去除率的影响,实验在如图1所示的装置中进行。

①在不同温度下反应相同时间,发现温度从60℃升高到95℃时,有机物去除率从29%增大到58%,其可能的原因是:MnO2的氧化能力随温度升高而增强;__。
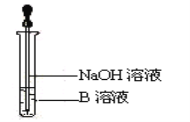
②废液因含有机物而呈现黑红色。有机物降解速率慢,难以观察气泡产生速率。降解一段时间,判断有机物浓度基本不变的依据是:三颈烧瓶内__。烧杯中盛放的试剂可以是__。
(2)降解一段时间后,加入硫铁矿(主要成分FeS2)将剩余MnO2还原,所得溶液中的主要离子有Fe3+、Mn2+、SO42-等,其离子方程式为__。
(3)滤液若用足量高纯度MnO2再次氧化降解,改变条件,有机物去除率可达66%。反应后过滤,所得滤渣经洗涤后,在本实验流程中可用于__。
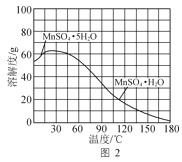
(4)MnSO4·H2O的溶解度曲线如图2所示。设计以过滤所得滤液为原料,进一步除去有机物等杂质并制取MnSO4·H2O晶体的实验方案:__,趁热过滤,用热的硫酸锰溶液洗涤,150℃烘干。[已知pH=5时Fe(OH)3和Al(OH)3沉淀完全;MnSO4·H2O分解温度为200℃。实验中必须使用的试剂:石灰石粉末、活性炭]
【答案】温度升高,反应速率加快 液体颜色不再变浅 NaOH溶液或石灰乳 2FeS2+15MnO2+28H+=2Fe3++15Mn2++4SO42-+14H2O 投入到降解阶段,作为氧化剂使用 在搅拌下向滤液中分批加入石灰石粉末,调节pH略大于5,过滤。向滤液中加入足量活性炭,充分吸附后过滤,将滤液在加压条件下,控制在180℃左右结晶
【解析】
由流程图可知,废液中含硫酸91%、难挥发有机物7%,通过加入软锰矿和水,将废液中的有机物降解,加入硫铁矿(主要成分FeS2)将剩余MnO2还原,滤液经过处理,将其他杂质离子除去,最终得到MnSO4H2O晶体。
(1)①升高温度,反应速率加快,在相同时间内有机物反应的更多,去除率增加;
②废液因含有机物而呈现黑红色,有机物越少,颜色越浅,故可通过颜色来判断反应情况;废液中有浓度较高的硫酸,可以与有机物发生氧化还原反应,浓硫酸被还原成SO2,可用碱液来吸收,所以烧杯中可以加入NaOH溶液或石灰乳;
(2)MnO2为氧化剂,FeS2为还原剂,在酸性条件下发生氧化还原反应。根据反应后溶液中有Fe3+、Mn2+、SO42-,可推断出反应方程式为:2FeS2+15MnO2+28H+=2Fe3++15Mn2++4SO42-+14H2O;
(3)由于投入MnO2的是足量的,反应后MnO2会有剩余,可以投入到降解阶段,作为氧化剂使用;
(4)滤液中含有Fe3+、Al3+有机物等杂质,先用石灰石调节溶液的pH至略大于5,使Fe3+、Al3+完全沉淀;有色的有机物杂质可用活性炭进行吸附。根据图2可知,温度越高,MnSO4H2O溶解度越小,但是200℃时MnSO4H2O会分解,所以结晶温度选择图中最高的180℃,常压下,水无法达到180℃,故此处要加压条件下结晶;

 名校课堂系列答案
名校课堂系列答案