题目内容
【题目】为研究沉淀的生成及其转化,某小组进行如图实验。关于该实验的分析不正确的是
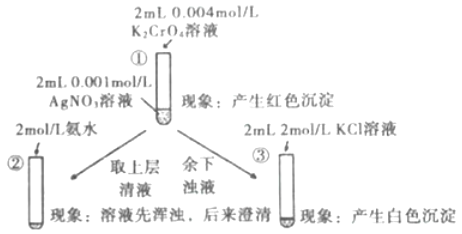
A.①浊液中存在平衡:Ag2CrO4(s)2Ag+(aq)+CrO42-(aq)
B.②中溶液变澄清的原因:AgOH+2NH3·H2O=[Ag(NH3)2]OH+2H2O
C.③中颜色变化说明有AgCl生成
D.该实验可以证明AgCl比Ag2CrO4更难溶
【答案】D
【解析】
A、反应①中沉淀是Ag2CrO4,存在溶解平衡:Ag2CrO4(s)![]() 2Ag+(aq)+CrO42-(aq),故A叙述正确;
2Ag+(aq)+CrO42-(aq),故A叙述正确;
B、反应①中存在溶解体系,即①的上层清液中存在Ag+,加入NH3·H2O,先发生Ag++NH3·H2O=AgOH↓+NH4+,继续滴加NH3·H2O,发生AgOH+2NH3·H2O=[Ag(NH3)2]OH+2H2O,因此溶液显变浑浊,再变澄清,故B叙述正确;
C、浊液中加入KCl,有白色沉淀产生,该沉淀为AgCl,故C叙述正确;
D、根据实验,加入KCl的浓度为2mol·L-1,比K2CrO4的浓度大的多,当c(Ag+)×c(Cl-)>Ksp时,就会有AgCl沉淀产生,因此本实验不能说明AgCl比Ag2CrO4更难溶,故D叙述错误;
答案选D。

【题目】CO2和CO可作为工业合成甲醇(CH3OH)的直接碳源,还可利用CO2据电化学原理制备塑料,既减少工业生产对乙烯的依赖,又达到减少CO2排放的目的。
(1)利用CO2和H2反应合成甲醇的原理为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
上述反应常用CuO和ZnO的混合物作催化剂。相同的温度和时间段内,催化剂中CuO的质量分数对CO2的转化率和CH3OH的产率影响的实验数据如下表所示:
ω(CuO)/% | 10 | 20 | 30 | 4b | 50 | 60 | 70 | 80 | 90 |
CH3OH的产率 | 25% | 30% | 35% | 45% | 50% | 65% | 55% | 53% | 50% |
CO2的转化率 | 10% | 13% | 15% | 20% | 35% | 45% | 40% | 35% | 30% |
由表可知,CuO的质量分数为________催化效果最佳。
(2)利用CO和H2在一定条件下可合成甲醇,发生如下反应:CO(g)+2H2(g)![]() CH3OH(g),其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是(______)
CH3OH(g),其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是(______)
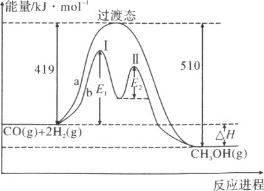
B.a反应正反应的活化能为510kJ·mol-1
C.b过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D.b过程使用催化剂后降低了反应的活化能和ΔH
E.b过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
(3)①在1L的恒定密闭容器中按物质的量之比1︰2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示,则压强P2________P1(填“>”、“<”或“=”);平衡由A点移至C点、D点移至B点,分别可采取的具体措施为________、________;在c点时,CO的转化率为________。
②甲和乙两个恒容密闭容器的体积相同,向甲中加入1molCO和2molH2,向乙中加入2molCO和4molH2,测得不同温度下CO的平衡转化率如图2所示,则L、M两点容器内压强:P(M)________2P(L);平衡常数:K(M)________K(L)。(填“>”、“<”或“=”)

(4)以纳米二氧化钛膜为工作电极,稀硫酸为电解质溶液,在一定条件下通入CO2进行电解,在阴极可制得低密度聚乙烯![]() (简称LDPE)。
(简称LDPE)。
①电解时,阴极的电极反应式是________。
②工业上生产1.4×102kg的LDPE,理论上需要标准状况下________L的CO2。
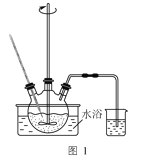
【题目】实验室制备溴苯的反应装置如图所示,回答下列问题:
已知:
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
水中的溶解度 | 微溶 | 微溶 | 微溶 |
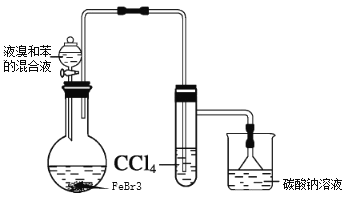
(1)实验装置c的作用为_______。
(2)写出实验室制备溴苯的反应方程式_______。
(3)本实验得到粗溴苯后,除去铁屑,再用如下操作精制:a蒸馏;b水洗;c用干燥剂干燥;d 10%NaOH溶液洗涤;e水洗,正确的操作顺序是________。
(4)本实验使用6mL无水苯、4.0mL液溴和少量铁屑,充分反应,经精制得到6.5mL的溴苯。则该实验中溴苯的产率是_______。