题目内容
6.X、Y为周期表VIA族的两种元素,下列叙述能说明X得电子能力比Y强的是( )| A. | X元素的电子层数比Y的电子层数多 | |
| B. | X的氢化物的沸点比Y的氢化物的沸点低 | |
| C. | X的气态氢化物比Y的气态氢化物稳定 | |
| D. | Y的单质能将X从H2X的溶液中置换出来 |
分析 根据单质之间的置换反应、气态氢化物的稳定性、最高价含氧酸的酸性、与氢化合的难易、元素周期律等来比较非金属性,以此来解答.
解答 解:A.X原子的电子层数比Y原子的电子层数多,为同主族元素,则Y的非金属性强,故A错误;
B.X的氢化物的沸点比Y的氢化物的沸点低,属于物理性质,与得失电子无关,故B错误;
C.X的气态氢化物比Y的气态氢化物稳定,则X的非金属性强,故C正确;
D.Y的单质能将X从H2X的溶液中置换出来,Y的非金属性强,得电子能力强,故D错误.
故选C.
点评 本题考查非金属性的比较,为高频考点,注意归纳非金属性比较的方法是解答的关键,明确同主族元素性质的变化规律即可解答,题目难度不大.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
16.某有机物的结构为HO-CH2CH=CHCH2-COOH,该有机物不可能发生的化学反应是( )
| A. | 水解 | B. | 酯化 | C. | 加成 | D. | 氧化 |
17.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1 molCl2参加反应转移电子数一定为2NA | |
| B. | 7.8gNa2O2中含有的阴离子数为0.1NA | |
| C. | 标准状况下,5.6 L四氯化碳含有的分子数为0.25NA | |
| D. | 1 mol FeCl3跟水完反应转化为氢氧化铁胶体,其中胶体粒子的数目为NA |
14.下列物质既含有离子键,又含有共价键的是( )
| A. | H2 | B. | NaOH | C. | MgCl2 | D. | HCl |
1.下列对化学反应的认识,错误的是( )
| A. | 会引起化学键的变化 | B. | 会产生新物质 | ||
| C. | 物质间必然发生电子转移 | D. | 必然伴随着能量的变化 |
18.下列有关物质的性质或应用的说法正确的是( )
| A. | 石油裂化的主要产品是甲烷、乙烯和苯 | |
| B. | 脂肪属于高分子化合物 | |
| C. | 盐析可提纯蛋白质并能保持蛋白质的生理活性 | |
| D. | 木糖醇(C5H12O5)是一种甜味剂,与葡萄糖互为同系物 |
15.38.4gCu与适量浓硝酸反应,当铜全部溶解后,共收集到标准状况下的气体22.4L(不考虑转化为N2O4),反应消耗的硝酸的物质的量是( )
| A. | 1mol | B. | 1.2 mol | C. | 2.2 mol | D. | 2.4 mol |
16.现有A、B、C、D四种金属片:
①把A、B用导线连接后同时浸入稀硫酸中,B表面变黑并逐渐溶解;
②把C、D用导线连接后同时浸入稀硫酸中,C发生氧化反应;
③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C.
根据上述情况,下列说法中正确的是( )
①把A、B用导线连接后同时浸入稀硫酸中,B表面变黑并逐渐溶解;
②把C、D用导线连接后同时浸入稀硫酸中,C发生氧化反应;
③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C.
根据上述情况,下列说法中正确的是( )
| A. | 如果把B、D用导线连接后同时浸入稀硫酸中,则金属片D上有气泡产生 | |
| B. | 在在①中,金属片B发生还原反应 | |
| C. | ②中,金属片C作正极 | |
| D. | 上述四种金属的活动性由强到弱的顺序是:A>B>C>D |
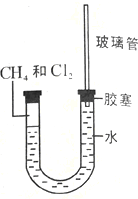 已知:卤素的氢化物易溶于水.某同学采用如图所示装置研究氯气与甲烷反应.实验时,往U型管的左端装入甲烷和氯气(体积比为1:4)的混合气体,并将该装置放置在光亮处,让混合气体缓慢地反应一段时间.根据要求回答问题:
已知:卤素的氢化物易溶于水.某同学采用如图所示装置研究氯气与甲烷反应.实验时,往U型管的左端装入甲烷和氯气(体积比为1:4)的混合气体,并将该装置放置在光亮处,让混合气体缓慢地反应一段时间.根据要求回答问题: A.氢原子数为十二 B.一氯取代物只有一种结构.
A.氢原子数为十二 B.一氯取代物只有一种结构.