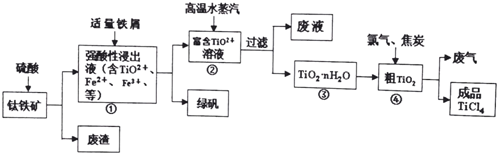
题目内容
16.某有机物的结构为HO-CH2CH=CHCH2-COOH,该有机物不可能发生的化学反应是( )| A. | 水解 | B. | 酯化 | C. | 加成 | D. | 氧化 |
分析 有机物的结构为HO-CH2-CH=CHCH2-COOH,含有官能团为-OH、-C=C-、-COOH,结合醇、烯烃、羧酸的性质来解答.
解答 解:HO-CH2CH=CHCH2-COOH含有碳碳双键,可发生加成、加聚和氧化反应,则C、D正确;
含有羧基,具有酸性,可发生酯化反应,则B正确,
不能发生水解反应,
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物中的官能团及性质的关系为解答的关键,侧重醇、烯烃、羧酸性质的考查,题目难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
7.如图是制备和研究乙炔性质的实验装置图.下列说法不正确的是( )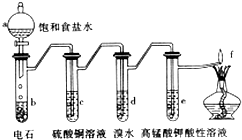

| A. | 制备乙炔的反应原理是CaC2+2H2O→Ca(OH)2+C2H2↑ | |
| B. | c的作用是除去影响后续实验的杂质 | |
| C. | d中的有机产物与AgNO3溶液混合能产生沉淀 | |
| D. | e中的现象说明乙炔不能被高锰酸钾酸性溶液氧化 |
4.如图为周期表中短周期的一部分,A、B、C三种元素的原子核外电子数等于B的质量数,B元素的原子核内质子数等于中子数,下列叙述正确的是( )
| A | C | |
| B |
| A. | B为第二周期的元素 | B. | C为ⅤA族元素 | ||
| C. | 三种元素中A可以为金属元素 | D. | C是化学性质最活泼的非金属 |
1.正己烷的碳链是( )
| A. | 直线形 | B. | 正四面体形 | C. | 锯齿形 | D. | 有支链的直线形 |
8.下列物质的类别与所含官能团都正确的是( )
| A. | 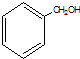 酚类-OH 酚类-OH | B. | HCOOH羧酸-COOH | C. |  醇类-OH 醇类-OH | D. | CH3-O-CH3 醚类 |
5.下列说法或表示方法正确的是( )
| A. | 由石墨比金刚石稳定可知:C(金刚石,s)=C(石墨,s)△H<0 | |
| B. | 强酸跟强碱反应放出的热量就是中和热 | |
| C. | 反应物的总能量低于生成物的总能量时,该反应一定不能发生 | |
| D. | 在101KPa、25℃时,1gH2完全燃烧生成气态水,放出120.9kJ热量,则氢气的燃烧热为241.8 kJ/mol |
6.X、Y为周期表VIA族的两种元素,下列叙述能说明X得电子能力比Y强的是( )
| A. | X元素的电子层数比Y的电子层数多 | |
| B. | X的氢化物的沸点比Y的氢化物的沸点低 | |
| C. | X的气态氢化物比Y的气态氢化物稳定 | |
| D. | Y的单质能将X从H2X的溶液中置换出来 |