题目内容
2.根据下列五种元素的电离能数据(单位:kJ/mol),回答下面各题.| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
A.Q和R B.S和T C.T和U D.R和U
(2)它们的氯化物的化学式,最可能正确的是B
A.QCl2 B.RCl C.SCl3 D.UCl4
(3)下列元素中,化学性质和物理性质最像T元素的是A
A.硼(1s22s22p1) B.铍(1s22s2)C.锂(1s22s1)D.氦(1s2)
分析 由元素的电离能可以看出,Q的电离能很大,可能为0族元素,R和U的第一电离能较小,最外层电子数为1,二者位于同一族,S的第一、第二电离能较小,最外层电子数为2,T的第一、第二、第三电离能较小,最外层电子数为3,以此判断元素在周期表中位置、化合价以及有关性质.
解答 解:由元素的电离能可以看出,Q的各电离能很大,可能为0族元素,R和U的第一电离能较小,最外层电子数为1,二者位于同一主族,S的第一、第二电离能较小,最外层电子数为2,T的第一、第二、第三电离能较小,最外层电子数为3,则
(1)R和U的第一电离能较小,最外层电子数为1,二者位于同一族,故答案为:D;
(2)由电离能可以看出,Q为各电离能都很大,可能为0族元素,R和U的第一电离能较小,最外层电子数为1,最高化合价为+1,S的第一、第二电离能较小,最外层电子数为2,最高化合价为+2,T的第一、第二、第三电离能较小,最外层电子数为3,最高化合价为+3,根据最高化合价可知,各氯化物分别是RCl、SCl2、TCl3、UCl,故答案为:B;
(3)T的第一、第二、第三电离能较小,最外层电子数为3,为第ⅢA族元素,化学性质和物理性质最像硼,故答案为:A.
点评 本题考查电离能知识,题目难度不大,注意原子的最外层电子与电离能以及化合价的关系.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.分子式为C8H10的苯的同系物的种数是( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
10.将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
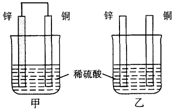

| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中铜片是正极,乙中铜片是负极 | ||
| C. | 两烧杯中硫酸溶液的浓度均下降 | D. | 产生气泡的速度甲比乙慢 |
17.利用原电池原理可以探究金属的活动性.
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计.锌片做负极(填“正”或“负”),锌片上发生的电极反应式是Zn-2e-=Zn2+;银片上发生的电极反应式是2H++2e-=H2↑.
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g.此时产生标准状况下氢气的体积为4.48L,通过导线的电子的物质的量为0.4mol.
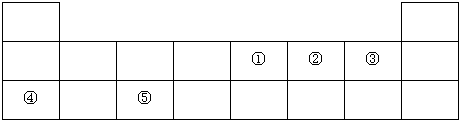
(3)为证明铁的金属活动性比铜强,某同学设计了如下一些方案.其中能证明铁的金属活动性比铜强的方案是①③④.(填序号)
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计.锌片做负极(填“正”或“负”),锌片上发生的电极反应式是Zn-2e-=Zn2+;银片上发生的电极反应式是2H++2e-=H2↑.
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g.此时产生标准状况下氢气的体积为4.48L,通过导线的电子的物质的量为0.4mol.
(3)为证明铁的金属活动性比铜强,某同学设计了如下一些方案.其中能证明铁的金属活动性比铜强的方案是①③④.(填序号)
| 方 案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气燃烧 | 产物分别为FeCl3和CuCl2 |
| ③将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| ④将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
7.使用氢氧燃料电池的汽车已在北京街头出现.下列有关该氢氧燃料电池的说法中,正确的是( )
| A. | H2在正极发生氧化反应 | |
| B. | 供电时的总反应是 2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$ 2H2O | |
| C. | 氢氧燃料电池中反应放出的热量转变为电能 | |
| D. | 产物是无污染的水,属于环境友好电池 |
 .
.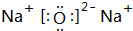 、
、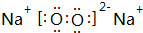 .(写两个)
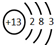
.(写两个) ,F元素原子的电子排布式1s22s22p63s23p5,E元素的原子结构示意图是
,F元素原子的电子排布式1s22s22p63s23p5,E元素的原子结构示意图是
 氮是地球上极为丰富的元素.
氮是地球上极为丰富的元素.