题目内容
【题目】下列各组物质中分子数相同的是( )
A.2L CO和2L CO2B.9gH2O和标准状况下 11.2LCO2
C.标准状况下1molO2和22.4LH2OD.0.2molH2和4.48LHCl气体
【答案】B
【解析】
A.相同条件下,相同体积的任何气体才具有相同的分子数,故A错误;
B.9gH2O的分子数N=![]() NA=0.5NA,标准状况下11.2LCO2的分子数N=
NA=0.5NA,标准状况下11.2LCO2的分子数N=![]() NA=0.5NA,所以9gH2O和标准状况下11.2LCO2中分子数相同,故B正确;
NA=0.5NA,所以9gH2O和标准状况下11.2LCO2中分子数相同,故B正确;
C.标准状况下1molO2的分子数为NA,标况下的水不是气态,所以22.4LH2O的分子数不是NA,故C错误;
D.0.2molH2的分子数为0.2NA,4.48LHCl气体在标况下的分子数才是0.2NA,而题干没指明状态,所以4.48LHCl气体的分子数不一定是0.2NA,故D错误;
故选B。

【题目】工业上制备 BaCl2·2H2O有如下两种途径。
途径 1:以重晶石(主要成分BaSO4)为原料,流程如下:
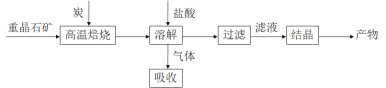
(1)写出“高温焙烧”时反应的化学方程式:_____________________________________。
(2)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为_____________。
(3)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,![]() =___________。 [Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
=___________。 [Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
途径 2:以毒重石(主要成分BaCO3,含Ca2+、Mg2+、Fe3+等杂质)为原料,流程如下:
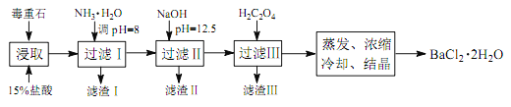
已知:Ksp(BaC2O4)=1.6×10-7, Ksp(CaC2O4)=2.3×10-9
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的 pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的 pH | 13.9 | 11.1 | 3.7 |
(4)为提高矿石的浸取率,可采取的措施是_________。
(5)加入 NH3·H2O 调节 pH=8 可除去___________(填离子符号),滤渣Ⅱ中含_________(填化学式)。加入 H2C2O4时应避免过量,原因是_________。
(6)重量法测定产品纯度的步骤为:准确称取 m g BaCl2·2H2O试样,加入100 mL水, 用3 mL 2 mol·L-1 的 HCl溶液加热溶解。边搅拌,边逐滴加入0.1 mol·L-1 H2SO4 溶液。待BaSO4完全沉降后,过滤,用0.01 mol·L-1 的稀H2SO4洗涤沉淀 3~4 次,直至洗涤液中不含Cl-为止。将沉淀置于坩埚中经烘干灼烧至恒重,称量为n g。则BaCl2·2H2O的质量分数为_________。
(7)20℃时,PbCl2(s)在不同浓度盐酸中的最大溶解量(单位:g·L-1)如图所示。下列叙述正确的是_______________
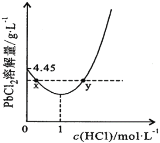
A.盐酸浓度越大,Ksp(PbCl2)越大
B.PbCl2能与一定浓度的盐酸反应
C.x、y两点对应的溶液中c(Pb2+)相等
D.往含Pb2+的溶液中加入过量浓盐酸,可将Pb2+完全转化为PbCl2(s)
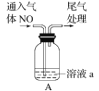
【题目】某小组以亚硝酸钠(NaNO2)溶液为研究对象,探究NO2-的性质。
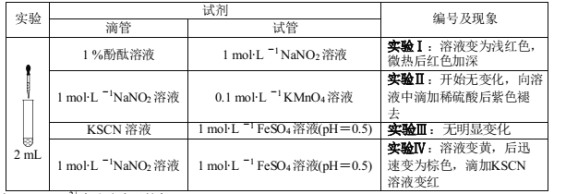
资料:[Fe(NO)] 2+在溶液中呈棕色。
(1)结合化学用语解释实验Ⅰ“微热后红色加深”的原因 ___;
(2)实验Ⅱ证明NO2-具有 ____性;
(3)实验Ⅳ证明NO2-具有_____性;写出此反应溶液先变黄后变成棕色的离子反应方程式 ____;
(4)探究实验Ⅳ中的棕色溶液
①为确定棕色物质是NO 与 Fe2+ 而非与 Fe3+ 发生络合反应的产物,设计如下实验,请补齐实验方案。
实验 | 溶液a | 现象 |
| 1mol/LFeSO4溶液(pH=0.5) | 溶液由________色迅速变为____色 |
__________________ | 无明显变化 |
②加热实验Ⅳ中的棕色溶液,有气体逸出,该气体在接近试管口处变为红棕色,溶液中有红褐色沉淀生成。解释上述现象产生的原因 ___ 。
【题目】实验室需要0.3 mol·L-1 NaOH溶液480 mL和一定浓度的盐酸溶液。根据这两种溶液的配制情况回答下列问题:

(1)如图所示的仪器中配制溶液肯定不需要的是_____________(填序号)。
(2)在配制NaOH溶液时:
填写下列表格:
应称取NaOH的质量/g | 应选用容量瓶的规格/mL |
__________________ | __________________ |
(3)容量瓶上需标有以下五项中的_________________(填序号)。
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(4)下列配制的溶液浓度偏低的是________________________(填序号)。
A.配制前,容量瓶中有少量蒸馏水
B.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
C.加蒸馏水时不慎超过了刻度线
D.定容时俯视刻度线
(5)下图为实验室某盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
盐酸
分子式:HCl
相对分子质量:36.5
密度:1.19g/mL
HCl的质量分数:36.5%
①该浓盐酸中HCl的物质的量浓度为_________molL-1。
②取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是____________
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有_________影响?(在横线上填“偏大”、“偏小”、“无影响”)。
Ⅰ溶液注入容量瓶前没有冷却至室温________
Ⅱ 定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水_________