��Ŀ����
����Ŀ������Ҫ��������Ӳ�ʻ����µĺϽ���Ȼ���к��ٿ����Ҫ�ɷ��������̵������Σ�FeWO4��MnWO4������������Si��P��As�Ļ�������ٿ�ұ���ٵĹ����������£�
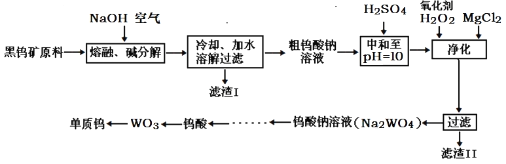
��֪��������I����Ҫ�ɷ���Fe2O3��MnO2��
�����������У������һ���⣬���ಽ�����ٵĻ��ϼ�δ�䣻
�۳���������������ˮ��
�ش��������⣺
��1�������Σ�FeWO4��MnWO4������Ԫ�صĻ��ϼ�Ϊ__________����д��MnWO4�����������·�����ֽⷴӦ����MnO2�Ļ�ѧ����ʽ____________��
��2�����������������������Һ�м������pH=10����Һ�е�����������ΪSiO32����HAsO32����HAsO42����HPO42���ȣ��������������У�����H2O2��Ŀ����__________�����������Ҫ�ɷ���__________��
��3���������ܱ���������H2��ԭWO3�ɵõ������٣��䷴Ӧ���̴��·�Ϊ�����Σ�������Ҫ�ɷ����¶ȵĹ�ϵ���±���
�¶� | 25�� �� 550�� �� 600�� �� 700�� |
��Ҫ�ɷ� | WO3 W2O5 WO2 W |
��֪���¶ȹ���ʱ��WO2(s)��ת��ΪWO2(g)��
WO2(s)+2H2(g) ![]() W(s)+2H2O(g) ��H =��66.0 kJ��mol��1
W(s)+2H2O(g) ��H =��66.0 kJ��mol��1
WO2(s) ![]() WO2(g) ��H =��203.9 kJ��mol��1
WO2(g) ��H =��203.9 kJ��mol��1
����700��ʱ��WO2(g)��H2(g)��Ӧ���ɹ���W(s)���Ȼ�ѧ����ʽΪ_____________��
��4����֪�������ƺ�����ƣ�CaWO4���������Եĵ���ʣ����ߵ��ܽ�Ⱦ����¶����߶���С����ͬ�¶����������ʵij����ܽ�ƽ����������ͼ����T1ʱKsp(CaWO4) =________��
����������Һ�м���ʯ����õ���������ƣ���T2ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ________��
��5�����õ�ⷨ���Դ�̼���٣�WC�������л����١����ʱ����̼�����������������������������Ϊ���Һ�������������Ტ�ų�CO2����������ӦʽΪ____________��
���𰸡� +6 2MnWO4 +O2 +4NaOH![]() 2MnO2 +2Na2WO4 + 2H2O ����HAsO32������HAsO42�� MgSiO3��MgHAsO4��MgHPO4 WO2(g)+2H2(g)
2MnO2 +2Na2WO4 + 2H2O ����HAsO32������HAsO42�� MgSiO3��MgHAsO4��MgHPO4 WO2(g)+2H2(g)![]() W(s)+2H2O(g) ��H =��137.9 kJ��mol��1 1��10��10 1��10��3 mol��L��1 WC +6H2O �C 10e�� �� H2WO4 + CO2��+10H+
W(s)+2H2O(g) ��H =��137.9 kJ��mol��1 1��10��10 1��10��3 mol��L��1 WC +6H2O �C 10e�� �� H2WO4 + CO2��+10H+
�������������̿�֪�������������������ơ�������Ӧ�����������������ƣ������̺��������Ʒ�Ӧ���������ƺ��������̣�ˮ��ʱ�����������������̲�����ˮ������������ˮ���ʹ��˺�õ�����Һ�������ƣ�����I����Ҫ�ɷ���Fe2O3��MnO2�������ƺ�Ũ���ᷴӦ��������������ƣ�����������⣬����+5�۵���Ϊ+6�ۣ������Ȼ�þ������������ˮ��MgSiO3��MgHAsO4�ȣ����ˣ���ҺΪ�����ƣ��ữ�����ȷֽ�����������ٺ�ˮ���û�ԭ����ԭ�������������٣���
��1��������FeWO4Ϊ���������������Σ�FeWO4��MnWO4���������̵Ļ��ϼ۶�Ϊ+2�ۣ��������Σ�FeWO4��MnWO4������Ԫ�صĻ��ϼ�Ϊ+x���������������ϼ۴�����Ϊ�㣬��+2+x+��-2����4=0�����x=+6����������ͼ��֪MnWO4���������ơ�������Ӧ���ɶ������̡�������ˮ����Ӧ�ķ���ʽΪ2MnWO4 +O2 +4NaOH![]() 2MnO2 +2Na2WO4 + 2H2O����2���������Ϸ���������H2O2��Ŀ���ǽ�HAsO32-������HAsO42-�����ӷ���ʽΪH2O2+HAsO32-��HAsO42-+H2O����ҺI�д���SiO32����HAsO32����HAsO42����HPO42�������ӣ���������pHֵ�����Ȼ�þ��Mg2+����SiO32����HAsO32����HAsO42����HPO42�������ӣ����������Ҫ�ɷ���MgSiO3��MgHAsO4��MgHPO4����3����֪����WO2(s)+2H2(g)
2MnO2 +2Na2WO4 + 2H2O����2���������Ϸ���������H2O2��Ŀ���ǽ�HAsO32-������HAsO42-�����ӷ���ʽΪH2O2+HAsO32-��HAsO42-+H2O����ҺI�д���SiO32����HAsO32����HAsO42����HPO42�������ӣ���������pHֵ�����Ȼ�þ��Mg2+����SiO32����HAsO32����HAsO42����HPO42�������ӣ����������Ҫ�ɷ���MgSiO3��MgHAsO4��MgHPO4����3����֪����WO2(s)+2H2(g) ![]() W(s)+2H2O(g) ��H =��66.0 kJ��mol��1����WO2(s)
W(s)+2H2O(g) ��H =��66.0 kJ��mol��1����WO2(s) ![]() WO2(g) ��H =��203.9 kJ��mol��1�����ݸ�˹���ɢ٣��ڼ��õ���700��ʱ��WO2(g)��H2(g)��Ӧ���ɹ���W(s)���Ȼ�ѧ����ʽΪWO2(g)+2H2(g)
WO2(g) ��H =��203.9 kJ��mol��1�����ݸ�˹���ɢ٣��ڼ��õ���700��ʱ��WO2(g)��H2(g)��Ӧ���ɹ���W(s)���Ȼ�ѧ����ʽΪWO2(g)+2H2(g)![]() W(s)+2H2O(g) ��H =��137.9 kJ��mol��1����4����T1ʱKSP��CaWO4��=c��Ca2+��c��WO42-��=1��10-5��1��10-5=1��10-10���ڽ���������Һ����ʯ���飬�������ֽⷴӦ���������ƺ���������ӷ�Ӧ��������Ƴ�������Ӧ�����ӷ���ʽΪWO42-+Ca��OH��2=CaWO4+2OH-������ͼ���֪���¶���KSP[Ca(OH)2]=c��Ca2+��c2��OH-��=1��10-6��(0.1)2=1��10-8�����Ը��¶��·�Ӧ��ƽ�ⳣ��K��
W(s)+2H2O(g) ��H =��137.9 kJ��mol��1����4����T1ʱKSP��CaWO4��=c��Ca2+��c��WO42-��=1��10-5��1��10-5=1��10-10���ڽ���������Һ����ʯ���飬�������ֽⷴӦ���������ƺ���������ӷ�Ӧ��������Ƴ�������Ӧ�����ӷ���ʽΪWO42-+Ca��OH��2=CaWO4+2OH-������ͼ���֪���¶���KSP[Ca(OH)2]=c��Ca2+��c2��OH-��=1��10-6��(0.1)2=1��10-8�����Ը��¶��·�Ӧ��ƽ�ⳣ��K��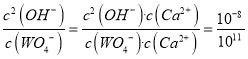 ��1��10��3 mol��L��1����5�������������Ტ�ų�CO2����˵��������WC�е�̼Ԫ��ʧȥ����ת��ΪCO2��Wת��Ϊ���ᣬ��˸���ԭ���غ��֪��������ӦʽΪWC+6H2O�C0e����H2WO4+CO2��+10H+��
��1��10��3 mol��L��1����5�������������Ტ�ų�CO2����˵��������WC�е�̼Ԫ��ʧȥ����ת��ΪCO2��Wת��Ϊ���ᣬ��˸���ԭ���غ��֪��������ӦʽΪWC+6H2O�C0e����H2WO4+CO2��+10H+��