题目内容
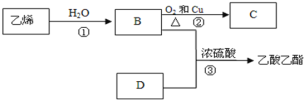
【题目】电子工业常用FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。从腐蚀废液(主要含FeCl3、FeCl2、CuCl2 )中回收铜,并重新获得FeCl3溶液。废液处理流程如下:

(1)步骤(Ⅰ)中分离溶液和沉淀的操作名称是____________________;
(2)沉淀B中主要含有铁和__________,气体D是_________________;
(3)写出步骤(Ⅲ)中生成FeCl3的化学方程式_____________;
(4)取少量最终所得溶液滴加___________,溶液呈红色,证明有Fe3+存在。
【答案】过滤 Cu(或铜) H2(或氢气) 2FeCl2 + Cl2 =2FeCl3 KSCN溶液
【解析】
腐蚀废液主要含FeCl3、FeCl2、CuCl2由转化关系图可知:向废液中加入过量的铁粉,发生反应Fe+2FeCl3=3FeCl2、Fe+CuCl2= FeCl2+Cu,则滤液A为FeCl2溶液,沉淀B为Cu和Fe,向沉淀B中加过量盐酸,发生反应Fe+2HCl= FeCl2+H2↑,则滤液C为FeCl2和HCl的混合溶液,气体D为H2,将滤液A和滤液C合并后通入足量的Cl2,发生反应2FeCl2+Cl2=2FeCl3,据此分析解答。
(1)步骤(Ⅰ)是将难溶物和溶液分离,操作名称是过滤;
(2)根据分析,沉淀B中主要含有Cu(或铜)、Fe,气体D是H2(或氢气);
(3)根据分析,步骤(Ⅲ)是将滤液A和滤液C合并后通入足量的Cl 2反应生成FeCl3,化学方程式为:2FeCl2+ Cl2=2FeCl3;
(4)Fe3+遇KSCN溶液变红,滴加KSCN溶液,溶液若呈红色,证明有Fe3+存在。

 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
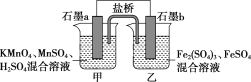
53天天练系列答案【题目】某同学在实验室进行铁盐与亚铁盐相互转化实验。
实验Ⅰ:将Fe3+转化为Fe2+

(1)Fe3+与Cu粉发生反应的离子方程式为_________________________________。
(2)某学生用对比实验法探究白色沉淀产生的原因,请填写实验万案:
实验方案 | 现象 | 结论 |
步骤1:取4mL①__________ mol/LCuSO4溶液,向其中滴加3滴0.1mol/LKSCN溶液 | 产生白色沉淀 | CuSO4溶液与KSCN溶液反应产生了白色沉淀 |
步骤2:取4mL②__________mol/LFeSO4 溶液向其中滴加3滴0.1mol/LKSCN溶液 | 无明显现象 |
查阅资料:
已知①SCN-的化学性质与I-相似 ②2Cu2++4I-=2CuI↓+I2
Cu2+与SCN-反应的离子方程式为③___________________________________。
实验Ⅱ:将Fe2+转化为Fe3+
实验方案 | 现象 |
向3mL0.1mol/LFeSO4溶液中加入 3mL0.5mol/L稀硝酸 | 溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色 |
探究上述现象出现的原因:
查阅资料:Fe2++NO![]() Fe(NO)2+(棕色)
Fe(NO)2+(棕色)
(3)用离子方程式解释NO产生的原因___________________________________。
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应Ⅰ:Fe2+与HNO3反应;反应Ⅱ:Fe2+与NO反应
①反应Ⅰ是一个不可逆反应,设计实验方案加以证明_____________________________。
②请用化学平衡移动原理解释溶液由棕色变为黄色的原因_____________________________。