题目内容
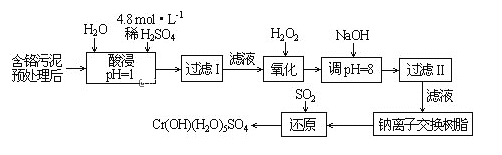
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | —— | —— | 4.7 | —— |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
(1)实验室用18.4 mol·L-1的浓硫酸配制250 mL 4.8 mol·L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需______________________。
(2)酸浸时,为了提高浸取率可采取的措施有___________________________。(写出两个措施)
(3)加入H2O2的作用是_____________________________________。
(4)加入NaOH溶液使溶液呈碱性,Cr2O72―转化为CrO42―。滤液Ⅱ中阳离子主要有______;但溶液的pH不能超过8,其理由是_______________。
(5)钠离子交换树脂的反应原理为:Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是___________________。
(6)写出上述流程中用SO2进行还原的离子方程式___________________________。
【答案】250mL容量瓶、烧杯 升高反应温度、增大固体颗粒的表面积、加快搅拌速度等 Cr3+转化为Cr2O72- Na+、Mg2+、Ca2+ pH超过8会使部分Al(OH)3溶解生成AlO2-,最终影响Cr(III)回收与再利用 Ca2+、Mg2+ 3SO2+ 2Na2CrO4+ 12H2O=2CrOH(H2O)5SO4↓+Na2SO4+ 2NaOH
【解析】
向含铬污泥中加入稀硫酸和水并将溶液pH调节为1,根据信息①知,硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+,然后过滤,向滤液中加入双氧水,发生2Cr3++3H2O2+H2O=Cr2O72-+8H+,Cr3+被氧化生成Cr2O72-,然后向溶液中加入NaOH溶液并调节溶液的pH=8,根据表中数据知,溶液中Fe3+、Al3+生成沉淀,且溶液中Cr2O72-转化为CrO42-,然后过滤,向滤液中加入钠离子交换树脂,除去Ca2+和Mg2+,最后向溶液中通入二氧化硫,发生反应2 CrO42-+3SO2+12H2O=2Cr(OH)(H2O)5SO4↓+SO42-+2OH-,以此来解答。
(1)配置一定物质的量浓度的溶液所需的玻璃仪器有:烧杯、玻璃棒、吸量管、容量瓶和胶头滴管,故答案为250mL容量瓶、胶头滴管;
(2)酸浸时,为了提高浸取率可采取的措施是升高反应温度、增大固体颗粒的表面积、加快搅拌速度等;故答案为升高反应温度、增大固体颗粒的表面积、加快搅拌速度等。
(3)双氧水有强氧化性,能氧化还原性的物质,Cr3+有还原性,Cr3+转化为Cr2O72-;故答案为Cr3+转化为Cr2O72-;
(4)碱性条件下Cr2O72-转化为CrO42-,加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-,滤液Ⅱ中阳离子主要有Na+、Ca2+、Mg2+;但溶液的pH不能超过8,其理由是pH超过8会使部分Al(OH)3溶解生成AlO2-,最终影响Cr(Ⅲ)回收与再利用,故答案为pH超过8会使部分Al(OH)3溶解生成AlO2-,最终影响Cr(III)回收与再利用;
(5)钠离子交换树脂交换 的离子是Mg2+、Ca2+,从而除去杂质离子Mg2+、Ca2+,故答案为Mg2+、Ca2+;
(6)上述流程中用SO2进行还原时发生反应的化学方程式为3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH,故答案为3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案【题目】以反应![]() 为例探究“外界条件对化学反应速率的影响"。实验时,分别量取
为例探究“外界条件对化学反应速率的影响"。实验时,分别量取![]() 溶液和酸性
溶液和酸性![]() 溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
编号 |
| 酸性 | 温度/℃ | ||
浓度 | 体积 | 浓度 | 体积 | ||
① | 0.10 | 2.0 | 0.01 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.01 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.01 | 4.0 | 50 |
下列说法不正确的是( )
A.实验①、②、③所加的![]() 溶液均要过量
溶液均要过量
B.实验①测得![]() 溶液的褪色时间为40 s,则这段时间内平均反应速率
溶液的褪色时间为40 s,则这段时间内平均反应速率![]()
C.实验①和②探究浓度对反应速率的影响,实验②、③探究温度对反应速率的影响
D.3组实验中均发现起初反应较慢,过了一会儿速率突然增大,可能是生成的![]() 对反应起催化作用
对反应起催化作用