题目内容
13.某物质在一定条件下按下式分解:2A═B↑+2C↑+2D↑,测得生成的混合气体在相同条件下密度是H2密度d倍,则A的式量为( )| A. | 2d | B. | 2.5d | C. | 5d | D. | 10d |
分析 根据相对密度计算生成的混合气体的平均摩尔质量,设A为2mol,则生成的混合气体为5mol,根据m=nM计算生成的混合气体总质量,根据质量守恒定律可知A的质量,再根据M=$\frac{m}{n}$计算A的摩尔质量,可以确定A的式量.
解答 解:生成的混合气体在相同条件下密度是H2密度d倍,则生成的混合气体的平均摩尔质量为2d g/mol,
设A为2mol,由方程式可知生成的混合气体为5mol,则生成的混合气体总质量=5mol×2d g/mol=10d g,根据质量守恒定律可知A的质量为10d g,则A的摩尔质量=$\frac{10dg}{2mol}$=5d g/mol,可以确定A的式量为5d,
故选:C.
点评 本题考查了阿伏伽德罗定律及其推论,明确相同条件下不同气体密度与其相对分子质量的关系是解本题关键,题目难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
3.已知丙二醇的结构简式为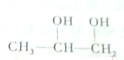 ,下列关于丙二醇的说法正确的是( )
,下列关于丙二醇的说法正确的是( )
 ,下列关于丙二醇的说法正确的是( )
,下列关于丙二醇的说法正确的是( )| A. | 丙二醇可发生消去反应生成丙炔 | |
| B. | 丙二醇可由丙烯在一定条件下与水加成制得 | |
| C. | 丙烯与溴水加成后,再与NaOH醇溶液共热水解可得丙二醇 | |
| D. | 丙二醇在铜存在下催化氧化可得到丙二醛 |
4.下列说法错误的是( )
| A. | 蒸馏时应调整温度计的水银球于蒸馏烧瓶支管口附近 | |
| B. | 红外光谱可以完全测定出有机物结构,判断出同分异构体 | |
| C. | 萃取是利用溶质在两种互不相溶的溶剂中溶解度的不同,使溶质从一种溶剂内转移到另一种溶剂的操作 | |
| D. | 常用质谱法进行有机物相对分子质量的测定 |
1.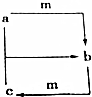 下列各组物质之间通过一步反应不能实现如图所示转化的是( )
下列各组物质之间通过一步反应不能实现如图所示转化的是( )
 下列各组物质之间通过一步反应不能实现如图所示转化的是( )
下列各组物质之间通过一步反应不能实现如图所示转化的是( ) | 选项 | a | b | c | m |
| A | 氢氧化钠 | 碳酸钠 | 碳酸氢钠 | 二氧化碳 |
| B | 硝酸 | 硝酸铁 | 硝酸亚铁 | 铁 |
| C | 硫酸铝 | 氢氧化铝 | 偏铝酸钠 | 氢氧化钠 |
| D | 氮气 | 一氧化氮 | 二氧化氮 | 氧气 |
| A. | A | B. | B | C. | C | D. | D |
18.某氯原子的质量为a g,12C原子的质量为b g,用NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
| A. | 氯原子的相对原子质量一定是$\frac{12a}{b{N}_{A}}$ | |
| B. | xg该氯原子物质的量一定是$\frac{x}{a{N}_{A}}$mol | |
| C. | 1mol该氯原子的质量是aNAg | |
| D. | yg该氯原子所含的氯原子数为$\frac{y}{a{N}_{A}}$ |
5.用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能还有杂质气体( )
①CO2 ②HCl ③H2O ④O2.
①CO2 ②HCl ③H2O ④O2.
| A. | ①②③④ | B. | ②③④ | C. | ②③ | D. | ①④ |
2.质量数为27的元素R,其核内有14个中子,则R可形成的离子为( )
| A. | R+ | B. | R2+ | C. | R3+ | D. | R2- |
3.2013年4月,俄罗斯公布了5个新探月计划,欲延续苏联时代辉煌.月球的土壤中吸附着数百万吨的${\;}_{\;}^{3}$He,每百吨${\;}_{\;}^{3}$He核聚变所释放出的能量相当于目前人类一年消耗的能量. 下列说法中正确的是( )
| A. | ${\;}_{\;}^{3}$He原子中的质子在原子核外空间内一定轨道上绕核高速运动 | |
| B. | ${\;}_{\;}^{3}$He原子不是微小的实心球体 | |
| C. | ${\;}_{\;}^{3}$He原子是不能再分的微粒 | |
| D. | ${\;}_{\;}^{3}$He的最外层电子数为2,故${\;}_{\;}^{3}$He具有较强的金属性 |