题目内容
4.写离子方程式a.氯化铝溶液中加入过量氨水的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+;b.碳酸钙与盐酸反应的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O.分析 a氯化铝溶液中加入过量氨水反应生成氢氧化铝和氯化铵;
b碳酸钙与盐酸反应生成氯化钙和二氧化碳和水.
解答 解:a氯化铝溶液中加入过量氨水反应生成氢氧化铝和氯化铵,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
b碳酸钙与盐酸反应生成氯化钙和二氧化碳和水,离子方程式:CaCO3+2H+=Ca2++CO2↑+H2O;
故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;CaCO3+2H+=Ca2++CO2↑+H2O.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意氢氧化铝只能溶解在强碱溶液中,题目难度不大.

练习册系列答案
相关题目
14.不能用离子方程式2H++CO32-=H2O+CO2↑表示的化学方程式是( )
| A. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | B. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | ||
| C. | K2CO3+2HCl═2KCl+H2O+CO2↑ | D. | Na2CO3+2HNO3═2NaNO3+H2O+CO2↑ |
15.短周期主族元素X、Y、Z、W原子序数依次增大,X-与氦原子电子层结构相同,Y原子核外L层电子数为8且Y与X同主族,Z原子的最外层电子数是内层电子总数的一半,W的最高正价与最低负价的代数和为4,下列说法正确的是( )
| A. | 微粒半径:X<X- | |
| B. | 简单氢化物的稳定性:Z比W的强 | |
| C. | W的氧化物的水化物的酸性一定比Z的强 | |
| D. | 最外层电子数由大到小的顺序为:Z、W、Y |
9.室温下向10mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
| A. | 溶液中导电粒子的数目减少 | |
| B. | 溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$值增大 | |
| C. | 醋酸的电离程度增大,c(H+)亦增大 | |
| D. | 再加入10 mL pH=11的NaOH溶液,酸与碱恰好完全反应 |
14.配制一定溶质质量分数的氯化钠溶液的一些操作步骤见下图,正确的操作顺序是( )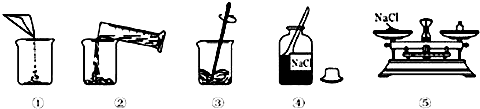

| A. | ④⑤①②③ | B. | ①②③④⑤ | C. | ③④①②⑤ | D. | ②①④③⑤ |

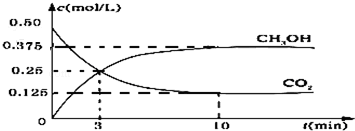
 .
.