题目内容
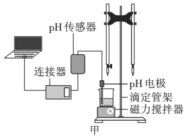
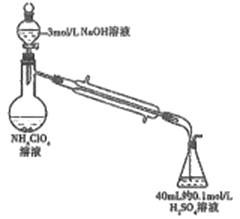
【题目】某小组利用下面的装置进行实验,②、③中溶液均足量,操作和现象如下表
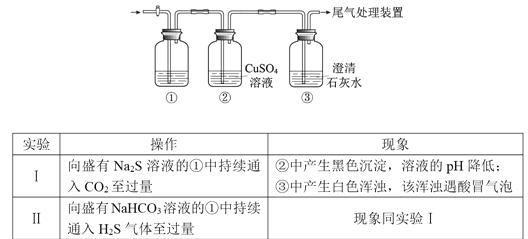
资料:CaS遇水完全水解
由上述实验得出的结论不正确的是
A.③中白色浑浊是CaCO3
B.②中溶液pH降低的原因是:H2S+Cu2+=CuS↓+2H+
C.实验①中CO2过量发生的反应是:CO2+H2O+S2-=CO32-+H2S
D.由实验I和II不能比较H2CO3和H2S酸性的强弱
【答案】C
【解析】
实验I:向盛有Na2S溶液的①中持续通入CO2至过量,②中产生黑色沉淀,溶液的pH降低,说明生成了硫化氢气体,同时生成了硫酸;③中产生白色沉淀,该浑浊遇酸冒气泡,说明二氧化碳被氢氧化钙溶液吸收生成了碳酸钙沉淀;
实验II:向盛有NaHCO3溶液的①中持续通入H2S气体至过量,②中产生黑色沉淀,溶液的pH降低,是因为过量的硫化氢气体与硫酸铜溶液反应生成了硫化铜黑色沉淀,同时生成了硫酸;③中产生白色沉淀,该浑浊遇酸冒气泡,说明反应生成了二氧化碳,被氢氧化钙溶液吸收生成了碳酸钙沉淀。
A.由上述分析可知,③中白色浑浊是CaCO3,不可能是CaS,CaS遇水完全水解,故A结论正确;
B.②中溶液降低的原因:H2S+Cu2+=CuS↓+2H+,产生黑色沉淀,溶液的pH降低,故B结论正确;
C.实验①中过量CO2发生的反应是2CO2+2H2O+S2-=2HCO3-+H2S,故C结论错误;
D.根据实验I和II中现象:I中通二氧化碳有硫化氢生成;II中通硫化氢有二氧化碳生成,故不能比较H2CO3和H2S酸性的强弱,故D结论正确;
答案为C。

练习册系列答案
相关题目