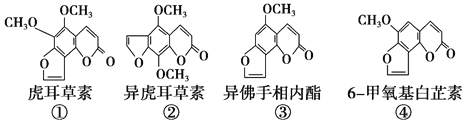
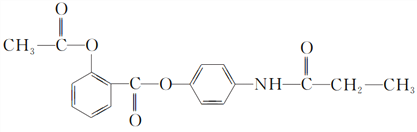
��Ŀ����
����Ŀ��
K��Fe��Ni��Ϊ��Ҫ�ĺϽ���ϣ��ڹ�ҵ�������Ƽ��������������Ź㷺����;����ش��������⣺
(1)KԪ�ش���Ԫ�����ڱ���_____ �������̬ԭ���У��������ռ�ݵĵ���������ͼΪ���ε��ܼ���______����
(2)KCl ��NaCl ��Ϊ��Ҫ�Ļ�ѧ�Լ���KCl ���۵����NaCl��ԭ��Ϊ___________��
(3)��ԭ�ӽṹ�Ƕȷ�����Fe3+��Fe2+���ȶ���ԭ����__________��
(4)NiSO4 ���ڰ�ˮ�γ�[Ni (NH3)6]SO4��
��д��һ����[Ni(NH3)6]SO4�е������ӻ�Ϊ�ȵ�����ķ��ӵķ���ʽ_________��
��1mol[Ni(NH3)6]SO4�к��ЦҼ�����ĿΪ___________��
��NH3 ��VSEPRģ��Ϊ_____ ������ԭ�ӵ��ӻ���ʽΪ_____�����ӻ����������Ϊ__________��
(5)K��Ni��F����Ԫ����ɵ�һ�־���ij����徧���ṹ��ͼ��ʾ����NAΪ�����ӵ�������ֵ���þ�����ܶȦ�=______g/cm3(�ô���ʽ��ʾ)��

���𰸡� s 4 K+�뾶����Na+�뾶��KCl����ľ�����С��NaCl����ľ����� ��̬Fe3+�ļ۵����Ų�ʽΪ3d5��Ϊ�����״̬�����ȶ� CX4��SiX4(X��ʾ±��ԭ��)����дһ�� 28NA �������� sp3 �γɦҼ������ɹµ��Ӷ� ![]()
��������(1). ��̬Kԭ�ӵļ۲�����Ų�ʽΪ4s1������KԪ�ش���Ԫ�����ڱ���s����s�ܼ��ĵ���������ͼΪ���Σ�����1s��2s��3s��4s��4�����ʴ�Ϊ��s��4��
(2). KCl��NaCl��Ϊ���Ӿ��壬���Ӿ�����۵�ߵ��ɾ����ܾ�������K+�뾶����Na+�뾶�� KCl����ľ�����С��NaCl����ľ����ܣ�����KCl���۵����NaCl���۵㣬�ʴ�Ϊ��K+�뾶����Na+�뾶��KCl����ľ�����С��NaCl����ľ�������
(3). ��̬Fe3+�ļ۵����Ų�ʽΪ3d5��Ϊ��������ȶ�״̬������̬Fe2+�ļ۵����Ų�ʽΪ3d6��������ʧȥ1�����ӣ��ʴ�Ϊ����̬Fe3+�ļ۵����Ų�ʽΪ3d5��Ϊ�����״̬�����ȶ���
(4). ��. ���ݵȵ�����Ķ��壬��SO42����Ϊ�ȵ�����ķ����У�CX4��SiX4(X��ʾ±��ԭ��)�����ʴ�Ϊ��CX4��SiX4(X��ʾ±��ԭ��)�ȣ���дһ������
��. [Ni(NH3)6]SO4��Ni2����6��NH3�γɵ�6����λ������������NH3�к���3��������SO42���к���4������������1mol[Ni(NH3)6]SO4�к�����������ĿΪ28NA���ʴ�Ϊ��28NA��
��. NH3��Nԭ�Ӽ۲���Ӷ���Ϊ4��VSEPRģ��Ϊ�������Σ�����ԭ�ӵ��ӻ���ʽΪsp3���ӻ�������������γ����������ɹµ��Ӷԣ��ʴ�Ϊ������������sp3���γɦҼ������ɹµ��Ӷ���
(5). �ɾ����ṹͼ��֪��ÿ����������2��Niԭ�ӡ�4��Kԭ�ӡ�8��Fԭ�ӣ������ܶ���=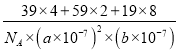 =
=![]() ���ʴ�Ϊ��
���ʴ�Ϊ�� ![]() ��
��

����Ŀ����һ̼��ѧ����ָ�Ժ�һ��̼ԭ�ӵĻ���������:CO2��CO��CH4��CH3OH����Ϊ��ʼ��Ӧ��,�ϳ�һϵ����Ҫ�Ļ���ԭ�Ϻ�ȼ�ϵĻ�ѧ��
��1����CO2��NH3Ϊԭ�Ϻϳ�����������CO2�ijɹ������������غϳ����е���Ҫ��Ӧ�ɱ�ʾ����:
��ӦI:2NH3(g)+CO2(g)=NH2COONH4(s)��H1
��ӦII:NH2COONH4(s)=CO(NH2)2(s)+H2O(g) ��H2=+72.49kJ/mol
�ܷ�Ӧ:2NH3(g)+CO2(g)==CO(NH2)2(s)+H2O(g) ��H3=-86.98kJ/mol
��ش���������:
�ٷ�ӦI����H1=______ kJ/mol
�ڷ�ӦIIһ����_________����������������������������������ڸ÷�Ӧ�Ľ��С�
��һ���¶���,�����Ϊ�̶����ܱ������а������Ƚ��з�ӦI,������˵����Ӧ�ﵽ��ƽ��״̬����__________�����������
A.��������ƽ����Է����������ٱ仯 B.������������ѹǿ���ٱ仯
C.2V��(NH3)=V��(CO2) D.�����ڻ��������ܶȲ��ٱ仯
�ܻ���Ϊ���ʱ,��һ�������������ܱ��������м���NH2COONH4����,�㹻��ʱ���Ӧ�Ƿ���ƽ��״̬? ___________��������������������
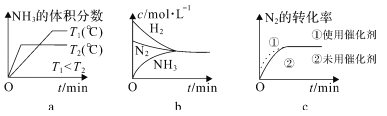
��2����CO2��H2����һ��������ܱ������У��������¶��·�����Ӧ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)�����CH3OH�����ʵ�����ʱ��ı仯����ͼ��
CH3OH(g)+H2O(g)�����CH3OH�����ʵ�����ʱ��ı仯����ͼ��
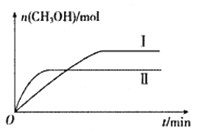
������I.II��Ӧ��ƽ�ⳣ����С��ϵΪKI_______KII������ >������<������=������
��һ���¶���,���ݻ���ͬ�ҹ̶��������ܱ������У������·�ʽ���뷴Ӧ�һ��ʱ���ﵽƽ�⡣
���� | �� | �� |
��Ӧ��Ͷ���� | 1molCO2��3molH2 | amolCO2��bmolH2 cmol CH3OH(g)��cmolH2O(g)(a��b��c����Ϊ��) |
��������ƽ��������ѹǿΪ��ʼ��0.8��,�������ƽ����������CH3OH(g)���������Ϊ_______��Ҫʹƽ��������������������ͬ��ֵ�����������,����ʼʱά�ֻ�ѧ��Ӧ���淴Ӧ�������,��������c��ȡֵ��ΧΪ________��
��3����TiO2/Cu2Al2O4Ϊ���������Խ�CO2��CH4ֱ��ת�������ᡣ�ڲ�ͬ�¶��´����Ĵ�Ч����������������ʵĹ�ϵ����ͼ,���������������Ҫȡ�����¶�Ӱ��ķ�Χ��________________��