题目内容
4.乙烯在不同的条件下可被氧化生成不同产物.如图所示: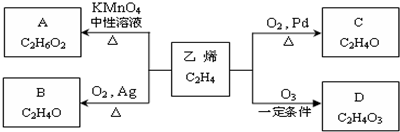
已知:取0.62g A与过量的金属钠完全作用后,生成224mL(标准状况)气体.B的沸点低(10.7℃),B不能发生银镜反应而C能.D有酸性、强氧化性,可用于消毒杀菌.
完成下列填空:
(1)写出结构简式.A
 DCH3COOOH
DCH3COOOH(2)写出C发生银镜反应的化学方程式.CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O
(3)在C的溶液中加入溴水实验现象:溴水褪色 解释产生该实验现象可能原因:乙醛与溴水发生氧化反应
(4)D可以和乙烯反应产生B,写出该反应的化学方程式.CH3COOOH+CH2=CH2C$\stackrel{催化剂}{→}$CH3COOH+
 .
.
分析 0.62g A的物质的量为$\frac{0.62g}{62g/mol}$=0.01mol,与过量的金属钠完全作用后,生成224mL(标准状况)气体,即生成氢气为$\frac{0.224L}{22.4L/mol}$=0.01mol,结合A的分子式可知,A分子中含有2个羟基,故A为乙二醇,结构简式为 ,由A与B、C的分子式可知,A分子内脱去1分子水生成B、C,而C能发生银镜反应而B不能,结合烯醇很不稳定,很快会发生异构化,形成稳定的羰基化合物,则B为
,由A与B、C的分子式可知,A分子内脱去1分子水生成B、C,而C能发生银镜反应而B不能,结合烯醇很不稳定,很快会发生异构化,形成稳定的羰基化合物,则B为 ,C为CH3CHO,乙烯发生氧化反应生成D,D一种同分异构体叫过氧乙酸,该同分异构体结构简式为CH3COOOH.
,C为CH3CHO,乙烯发生氧化反应生成D,D一种同分异构体叫过氧乙酸,该同分异构体结构简式为CH3COOOH.
解答 解:(1)0.62g A的物质的量为$\frac{0.62g}{62g/mol}$=0.01mol,与过量的金属钠完全作用后,生成224mL(标准状况)气体,即生成氢气为$\frac{0.224L}{22.4L/mol}$=0.01mol,结合A的分子式可知,A分子中含有2个羟基,故A为乙二醇,结构简式为 ,由A与B、C的分子式可知,A分子内脱去1分子水生成B、C,而C能发生银镜反应而B不能,结合烯醇很不稳定,很快会发生异构化,形成稳定的羰基化合物,则B为
,由A与B、C的分子式可知,A分子内脱去1分子水生成B、C,而C能发生银镜反应而B不能,结合烯醇很不稳定,很快会发生异构化,形成稳定的羰基化合物,则B为 ,C为CH3CHO,
,C为CH3CHO,
(1)由上述分析可知,A的结构简式为 ,D的结构简式为:CH3COOOH,故答案为:
,D的结构简式为:CH3COOOH,故答案为: ;CH3COOOH;
;CH3COOOH;
(2)C发生银镜反应的化学方程式为:CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O,故答案为:CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O;
(3)乙醛中含有醛基,具有还原性,溴水具有氧化性,两者反应使溴水褪色,故答案为:溴水褪色,乙醛与溴水发生氧化反应;
(4)乙烯与过氧乙酸反应生成环氧乙烷和乙酸,化学反应方程式为:CH3COOOH+CH2=CH2C$\stackrel{催化剂}{→}$CH3COOH+ ,故答案为:CH3COOOH+CH2=CH2C$\stackrel{催化剂}{→}$CH3COOH+
,故答案为:CH3COOOH+CH2=CH2C$\stackrel{催化剂}{→}$CH3COOH+ .
.
点评 本题考查有机物推断,计算确定A为乙二醇是关键,再结合B、C的能否发生银镜反应推断二者结构,存在考查学生的分析推理能力,难度中等.

 中考解读考点精练系列答案
中考解读考点精练系列答案| A. | 加入适量醋酸钠晶体后,两溶液的pH均增大 | |
| B. | 将温度升高至50℃,两溶液的pH均不变 | |
| C. | 加水稀释至原体积的2倍后,两溶液的pH均减小 | |
| D. | 加入足量锌粉充分反应后,两溶液产生氢气一样多 |
| A. | 推广使用燃煤脱硫技术,防止SO2污染 | |
| B. | 采用绿色化学生产工艺,提高原子利用率 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 加大石油、煤炭的开采力度,增加化石燃料的供应量 |
| A. | 加入铝粉放出H2的溶液中:Al3+、K+、SO42-、Cl- | |
| B. | 1.0 mol•L-1的KNO3溶液中:Na+、Fe2+、Cl-、SO42- | |
| C. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| D. | 水电离产生的c(OH-)=10-12 mol•L-1的溶液中:K+、Cu2+、SO42-、NO3- |
| A. | 向硫酸铜溶液中加入过量的NaHS溶液:Cu2++2HS-→CuS↓+H2S↑ | |
| B. | Fe3O4溶解在过量的稀硝酸中:Fe3O4+8H+→Fe2++2Fe3++4H2O | |
| C. | 碳酸氢铵溶液与苛性钾溶液混和共热:NH4++OH-→NH3↑+H2O | |
| D. | 将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O→SO32-+2HClO |
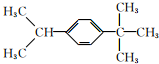 的一氯化物共有(不考虑立体异构)( )
的一氯化物共有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 7种 |
| A. | 某烷烃CnH2n+2的一个分子中,含有共价键的数目是3n+1 | |
| B. | 用HNO3酸化的AgNO3溶液检验CCl4中是否含有氯元素 | |
| C. | 红热的铜丝可以和乙醇发生置换反应产生氢气 | |
| D. | 石油化工得到的产品均为液体,煤化工得到的产品有液体也有固体 |
| A. | 氧化钠、氧化铁、氧化镁均为碱性氧化物 | |
| B. | 离子键、共价键、金属键、氢键均为化学键 | |
| C. | 氨水、水玻璃、水银、聚乙烯均为混合物 | |
| D. | 水能、风能、生物质能、核能均为可再生能源 |
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |