题目内容
【题目】氮及其化合物是重要的化工原料
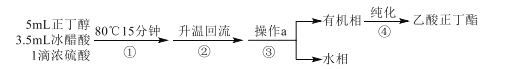
(1)利用图所示装置及药品制取氨气。
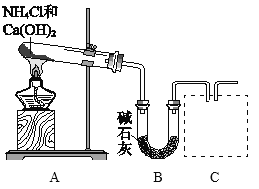
①A中制氨气的化学方程式是________。
②C处是用集气瓶收集氨气的装置,请绘出装置图。________
③证明氨气已集满的操作和现象是________。
(2)氨经催化氧化可制备硝酸,其过程中涉及如下反应。4NH3 + 5O2 ![]() 4NO + 6H2O
4NO + 6H2O
①作为氧化剂的物质是______,氮元素的化合价______(填“升高”或“降低”)。
②若反应中消耗了4 mol NH3,则生成NO的物质的量为______ mol,转移电子的物质的量为______ mol。
(3)含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下:
![]()
请回答:
①过程Ⅲ发生化合反应的化学方程式为______。
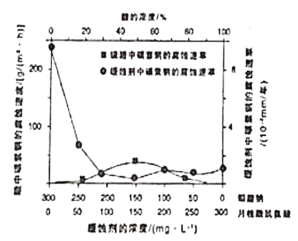
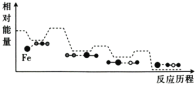
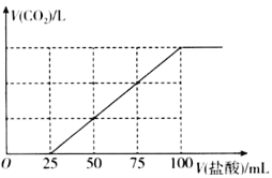
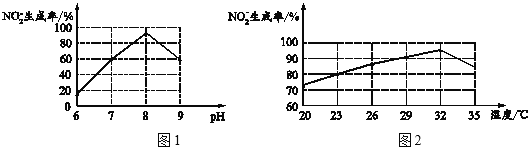
②根据图1和图2,推断使用亚硝化菌的最佳条件为______。
③利用微生物处理含氮废水的优点为______。
【答案】2NH4Cl+Ca(OH)2 =CaCl2+2NH3+2H2O  (短进长出,且有瓶塞) 将湿润的红色石蕊试纸靠近C与右侧的导管口,试纸变成蓝色 O2 升高 4 20 2HNO2+O2=2HNO3 pH=8、32℃ 反应条件温和,过程中使用的物质无毒无害,终产物无污染
(短进长出,且有瓶塞) 将湿润的红色石蕊试纸靠近C与右侧的导管口,试纸变成蓝色 O2 升高 4 20 2HNO2+O2=2HNO3 pH=8、32℃ 反应条件温和,过程中使用的物质无毒无害,终产物无污染
【解析】
(1)①实验室用氯化铵晶体与氢氧化钙反应制备氨气;
②氨气的密度小于空气的密度,因此用集气瓶收集氨气时导管短进长出;
③实验室常用湿润的红色石蕊试纸检验氨气是否收集满;
(2)①氨气催化氧化的反应中氨气中的N元素为-3价,反应N元素变为+2价,化合价升高,失去电子,被氧化,氨气作还原剂,O元素由0价降低到-2价,化合价降低,得到电子,被还原,氧气作氧化剂;
②根据方程式可知,反应消耗4mol氨气时,生成NO 4mol,电子转移20mol;
(3)①过程Ⅲ中亚硝酸与氧气反应生成硝酸;
②根据图1可知当pH=8时,NO2-的生成率最大;由图2可知当温度为32℃时,NO2-的生成率最大;
③可从反应条件、环境污染、处理效果等方面分析。
(1)①实验室用氯化铵晶体与氢氧化钙反应制备氨气,反应方程式为:2NH4Cl+Ca(OH)2 =CaCl2+2NH3+2H2O;
②氨气的密度小于空气的密度,因此用集气瓶收集氨气时导管短进长出,装置为: ;
;
③实验室常用湿润的红色石蕊试纸检验氨气是否收集满,过程为:将湿润的红色石蕊试纸靠近C与右侧的导管口,试纸变成蓝色;
(2)①反应中N元素化合价由-3价升高到+2价,化合价升高;O元素由0价降低到-2价,化合价降低,得到电子,被还原,氧气作氧化剂;
②根据方程式可知,反应消耗4mol氨气时,生成NO 4mol,电子转移20mol;
(3)①过程Ⅲ中亚硝酸与氧气反应生成硝酸,反应方程式为:2HNO2+O2=2HNO3;
②根据图1可知当pH=8时,NO2-的生成率最大;由图2可知当温度为32℃时,NO2-的生成率最大,因此使用亚硝化菌的最佳条件为pH=8,温度为32℃;
③分析微生物对含氮废水进行处理的流程可知,微生物处理含氮废水的优点为反应条件温和,过程中使用的物质无毒无害,终产物无污染。

【题目】苯甲酸又称安息香酸(C6H5COOH),可用于合成纤维、树脂涂料等也可作为药物或防腐剂使用,有抑制真菌、细菌生长的作用。实验室中由甲苯制备苯甲酸的实验如下:
查阅资料:
①苯甲酸是一元有机弱酸不易被氧化。在水中溶解度:0.35g(25℃)、2.7g(80℃)、5.9g(100℃)。甲苯易溶于有机溶剂,不溶于水。
②
相对分子质量 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) | |
苯甲酸 | 122 | 122.4 | 249 | 1.3 |
甲苯 | 92 | -95 | 110.6 | 0.9 |
实验步骤:
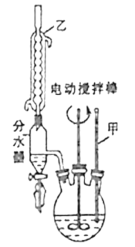
第一步:将9.2g甲苯和硫酸酸化的KMnO4溶液(过量)置于如图的三颈烧瓶中,加热保持反应物溶液温度在90℃左右至反应结束,主要反应为5C6H5CH3+6KMnO4+9H2SO4![]() 5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
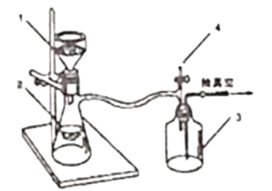
第二步:将反应后混合液趁热过滤滤液冷却后用硫酸酸化用如图装置抽滤得粗产品;(抽滤又称减压过滤利用抽气泵使抽滤瓶中的压强降低达到固液分离的目的。)
第三步:粗产品用水洗涤2到3次,干燥称量得固体![]() .
.
请回答下列问题:
(1)图1中装置乙的名称为___。
(2)分水器的作用是分离出水其主要目的是___,判断该反应进行完全的实验现象是___。
(3)实验第二步中,趁热过滤的原因是___,采用抽滤的优点是____。停止抽滤时先旋开图2中4处的旋塞恢复常压,然后关闭抽气泵,装置3起到的作用是____。
(4)第三步证明粗产品洗涤干净的方法是___。
(5)苯甲酸的产率为____。
(6)结合下列试剂和用品设计最简单实验验证苯甲酸是弱酸,具体操作为__。
0.010mol·L-1的苯甲酸溶液;0.010mol·L-1的苯甲酸钠溶液;0.010mol·L-1的氢氧化钠溶液;0.010mol·L-1的盐酸溶液;广泛pH试纸;甲基橙,酚酞(仪器任选)。