题目内容
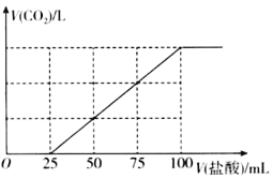
【题目】向100mlNaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示。下列判断正确的是( )
A.通入CO2后,所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3)=1:1
B.通入CO2在标准状况下的体积为448mL
C.通入CO2后,所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3)=1:3
D.原NaOH溶液的浓度为0.2mol/L
【答案】D
【解析】
根据图像可知,加盐酸的体积0~~25mL时,无气体生成,发生反应为Na2CO3+HCl═NaHCO3+NaCl,加盐酸的体积为25mL~~100 mL时,产生气体,发生的反应为NaHCO3+HCl═CO2↑+NaCl+H2O。
A、根据图像可知,加盐酸的体积0~~25mL时,无气体生成,发生反应为Na2CO3+HCl═NaHCO3+NaCl,消耗盐酸的物质的量为0.2mol/L×0.025L=0.005mol,所以n(Na2CO3)=0.005mol;加入盐酸100mL时恰好完全反应,此时溶质只有氯化钠,n(Na+)=n(Cl-)=0.2mol/L×0.1L=0.02mol,则n(NaHCO3)=0.02mol-0.005mol×2=0.01mol,通入CO2后,所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3)=2:1,故A错误;
B、加盐酸的体积为25mL~~100 mL时,产生气体,发生的反应为NaHCO3+HCl═CO2↑+NaCl+H2O,此反应消耗盐酸的物质的量是0.2mol/L×0.075L=0.015mol,放出CO2在标准状况下的体积为0.015mol ×22.4L/mol=0.336L=336mL,所以氢氧化钠溶液通入CO2在标准状况下的体积为336mL,故B错误;
C、假设NaOH与CO2气体反应所得溶液中只有Na2CO3,则开始阶段发生反应:Na2CO3+HCl=NaHCO3+NaCl,由方程式可知,前后两个阶段消耗盐酸的体积应相等,而实际生成二氧化碳消耗的盐酸体积多,故NaOH与CO2气体反应所得溶液中溶质为Na2CO3、NaHCO3,没有氢氧化钠,故C错误;
D、加入100mL盐酸时二氧化碳的体积达最大,此时溶液为NaCl溶液,根据元素守恒,所以n(NaOH)=n(NaCl)=n(HCl)=0.1L×0.2mol/L=0.02mol,所以c(NaOH)=![]() =0.2mol/L,故D正确。
=0.2mol/L,故D正确。