题目内容
4.如表实验“操作和现象”与“结论”对应关系正确的是( )| 操作和现象 | 结论 | |
| A | 向NaCl溶液中先滴加少量AgNO3溶液,后滴加少量NaI溶液,先有白色沉淀,后变成黄色沉淀 | 说明Ksp(AgI)<Ksp(AgCl) |
| B | 将SO2通入酸性KMnO4溶液中,紫色褪去 | 说明SO2具有漂白性 |
| C | 向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 | 说明氧化性:Cu2+>Fe3+ |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有Ag+ |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溶度积常数大的物质能转化为溶度积常数小的物质,生成白色沉淀为AgCl,然后发生沉淀转化;
B.二氧化硫具有还原性,能被强氧化性物质氧化;
C.向FeCl3、CuCl2混合溶液加铁粉,先发生Fe与铁离子的反应;
D.沉淀可能为硫酸钡.
解答 解:A.溶度积常数大的物质能转化为溶度积常数小的物质,生成白色沉淀为AgCl,然后发生沉淀转化,生成黄色沉淀AgI,则说明Ksp(AgI)<Ksp(AgCl),故A正确;
B.高锰酸钾溶液具有强氧化性,二氧化硫能被酸性高锰酸钾溶液氧化,酸性高锰酸钾被还原,所以酸性高锰酸钾溶液褪色,则二氧化硫体现还原性,故B错误;
C.向FeCl3、CuCl2混合溶液加铁粉,先发生Fe与铁离子的反应生成亚铁离子,再发生Fe与氯化铜反应,则说明氧化性:Cu2+<Fe3+,故C错误;
D.向某溶液先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成,沉淀可能为硫酸钡,也可能为AgCl,该溶液中可能含有Ag+,还有可能亚硫酸根或亚硫酸氢根离子被氧化生成硫酸根离子,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及沉淀转化、二氧化硫的性质、氧化性强弱比较、离子检验等知识点,明确实验原理及物质性质是解本题关键,易错选项是D,注意应该用盐酸酸化的氯化钡溶液检验硫酸根离子,为易错点.

练习册系列答案
相关题目
14.如图所示,试管中盛有已检出部分离子的某溶液,下列推理正确的是( )


| A. | 向该溶液中加入Mg有H2逸出 | |
| B. | 向该溶液中加入少量FeCl2,其离子反应方程式为:2NO3-+6I-+4H2O | |
| C. | 该溶液还可能大量存在MnO4-、ClO- | |
| D. | 向该溶液中逐滴加入Na2CO3溶液至过量,既有气体逸出又有沉淀生成 |
12.下列各组有机物,不管它们以何种比例混合,只要物质的量一定,则完全燃烧时消耗氧气为一定值的是( )
| A. | C4H6 C3H8 | B. | C5H10 C6H6 | C. | C2H6O C2H4O2 | D. | C3H6 C3H8O |
9.2L密闭容器中,反应2SO2(g)+O2(g)═2SO3(g),经一段时间后SO3的浓度增加了0.8mol,在这段时间内用O2表示的反应速率为0.4mol•L-1•min-1,则这段时间为( )
| A. | 0.5s | B. | 1s | C. | 30s | D. | 60s |
14.在某溶液中先滴加稀硝酸,再滴加氯化钡溶液,有白色沉淀产生,溶液中( )
| A. | 一定含有SO42- | B. | 一定含有Ag+ | ||
| C. | 一定含有Ag+和SO42- | D. | 可能含有Ag+或SO42- |
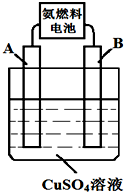 能源的开发、利用与人类社会的可持续发展息息相关,怎样充分利用好能源是摆在人类面前的重大课题.
能源的开发、利用与人类社会的可持续发展息息相关,怎样充分利用好能源是摆在人类面前的重大课题.
 .
. .
.