题目内容
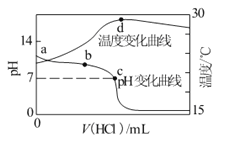
【题目】(1)地球上的能源主要源于太阳,绿色植物的光合作用可以大量吸收CO2以减缓温室效应,主要过程可以描述分为下列三步(用“C5”表示C5H10O4,用“C3”表示C3H6O3):
Ⅰ、H2O(l)═2H+(aq)+ ![]() O2(g)+2e﹣△H=+284kJ/mol
O2(g)+2e﹣△H=+284kJ/mol
Ⅱ、CO2(g)+C5(s)+2H+(aq)═2C3+(s)△H=+396kJ/mol
Ⅲ、12C3+(s)+12e﹣═C6H12O6(葡萄糖、s)+6C5(s)+3O2(g)△H=﹣1200kJ/mol
写出绿色植物利用水和二氧化碳合成葡萄糖并放出氧气的热化学方程式_________.
(2)降低大气中CO2的含量及有效地开发利用CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H=﹣49.0kJ/mol.
CH3OH(g)+H2O(g)△H=﹣49.0kJ/mol.
测得CO2和CH3OH(g)的浓度随时间变化如图1所示
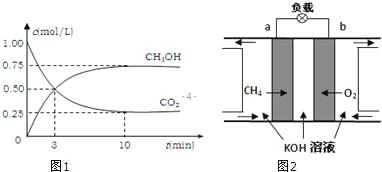
①一定温度下,不能说明该反应达到平衡状态的是:_________(填序号)
a.体系的压强不再改变
b.体系的密度不再改变
c.各气体的浓度不再改变
d.各气体的质量分数不再改变
e.反应速率v(CO2)正∶v(H2)逆=1∶3
②从反应开始到平衡,氢气的平均反应速率v(H2)=________mol/(Lmin);
③氢气的转化率=____________;
④该反应的平衡常数为K=_________保留三位有效数字);
⑤下列措施中能使平衡体系中n(CH3OH)/ n(CO2)增大的是________.
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出去 D.再充入1mol CO2和3mol H2
⑥当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2.则c1____c2的关系(填>、<、=).
(3)减少温室气体排放的关键是节能减排,大力开发利用燃料电池就可以实现这一目标.如图2所示甲烷燃料电池(在上面).请回答:
①通入甲烷一极的电极反应式为___________;
②随着电池不断放电,电解质溶液的pH______(填“增大”、“减小”或“不变”).
③通常情况下,甲烷燃料电池的能量利用率____(填“大于”、“小于”或“等于”)甲烷燃烧的能量利用率.
④用该燃料电池以石墨电极电解2.0L 0.25 mol·L-1 CuSO4溶液,5min后在一个电极上有6.4gCu析出。则阳极的电极反应式为____________________; 此时得到的O2在标准状况下的体积为______L;向电解后的溶液中加入下列哪种物质可使电解质溶液恢复原来的浓度:____________
A. CuSO4 B.H2O C.CuO D.CuCO3
【答案】6CO2(g)+6H2O(l)=C6H12O6(s)+6O2(g)△H=+2880 kJmol﹣1b0.22575%K=5.33(mol/L)-2CD<CH4-8e-+10OH-=CO32-+7H2O减小大于4OH--4e-=2H2O+O2↑或2H2O-4e-==O2↑+4H+1.12CD
【解析】
(1)依据盖斯定律由题干所给的热化学方程式,结合盖斯定律计算(①+②)×6+③得到绿色植物利用水和二氧化碳合成葡萄糖并放出氧气的热化学方程式,
6CO2(g)+6H2O(g)=C6H12O6(葡萄糖、s)+6O2(g)△H=[(+284KJ/mol)+(+396KJ/mol)]×6+(-1200KJ/mol)=+2880KJ/mol;
则△H=[(+284KJ/mol)+(+396KJ/mol)]×6+(-1200KJ/mol)=+2880KJ/mol,即6CO2(g)+6H2O(l)=C6H12O6(s)+6O2(g)△H=+2880 kJmol-1;(2)①a.反应体系气体反应物与生成物的系数和不等,则恒容条件下压强不再改变,可说明是平衡状态,故a正确;b.气体的总质量和体积始终不变,体系的密度始终不变改变,不能说明是平衡状态,故b错误;c.各气体的浓度不再改变,量不再随时间改变,可说明是平衡状态,故c正确;d.各气体的质量分数不再改变,可说明是平衡状态,故d正确;e.反应速率v(CO2)正∶v(H2)逆=1∶3,可说明是平衡状态,故e正确;答案为b。
②利用三段式解题法计算
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),
CH3OH(g)+H2O(g),
开始(mol/L):13 0 0
变化(mol/L):0.75 2.25 0.750.75
平衡(mol/L):0.25 0.75 0.750.75
从反应开始到平衡,氢气的平均反应速率v(H2)=![]() =0.225 molL-1min-1;
=0.225 molL-1min-1;
③氢气的转化率=![]() ×100%=75%;
×100%=75%;
④平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,则K=![]()
=![]() =5.33;
=5.33;
⑤要使n(CH3OH)/n(CO2)增大,应使平衡向正反应方向移动;A.因正反应放热,升高温度平衡向逆反应方向移动,则比值减小,故A错误;B.充入He(g),使体系压强增大,但对反应物质来说,浓度没有变化,平衡不移动,比值不变,故D错误.故B错误;C.将H2O(g)从体系中分离,平衡向正反应方法移动,比值增大,故C正确;D.再充入1mol CO2和3mol H2,增大反应物浓度,平衡向正反应方向移动,则比值增大,故D正确;故答案为CD;
⑥若是恒容密闭容器、反应后整个体系的压强比之前来说减小了,加入氢气虽然正向移动,平衡移动的结果是减弱这种改变,而不能消除这种改变,即虽然平衡正向移动,氢气的物质的量在增加后的基础上减小,但是CO2(g)浓度较小、CH3OH(g) 浓度增大、H2O(g)浓度增大,且平衡常数不变达到平衡时H2的物质的量浓度与加氢气之前相比一定增大,故c1<c2;
(3)①在碱性溶液中,负极上投放燃料甲烷,发生失电子发生氧化反应:CH4-8e-+10OH-═CO32-+7H2O;
②燃料电池的总反应是:CH4+2O2+2KOH═K2CO3+3H2O,消耗氢氧根离子,所以碱性减弱,pH减小;
③甲烷燃烧时要放出热量、光能,所以燃料电池中甲烷的利用率比甲烷燃烧的能量利用率高;
④阳极发生氧化反应,电极反应式为4OH--4e-=O2↑+2H2O;根据阴极反应:Cu2++2e-═Cu,当有6.4gCu即0.1mol生成时,反应所转移的电子的物质的量是0.2mol,得到氧气的体积为:![]() ×22.4=1.12L,根据电解的离子方程式2Cu2++2H2O
×22.4=1.12L,根据电解的离子方程式2Cu2++2H2O![]() 2Cu+O2↑+4H+,反应生成铜的物质的量为:0.1mol,相当于减少了0.1molCuO,故向电解后的溶液中加入0.1molCuO可使电解质溶液恢复原来的浓度,故答案为C。
2Cu+O2↑+4H+,反应生成铜的物质的量为:0.1mol,相当于减少了0.1molCuO,故向电解后的溶液中加入0.1molCuO可使电解质溶液恢复原来的浓度,故答案为C。

【题目】早期发现的一种天然二十面体准晶颗粒由Al、Cu.Fe三种金属元素组成,回答下列问题:
(1)①铜元素位于周期表中_____区。Cu2+离子的价层轨道表示式为____。
②锰、铁、钴三种元素的逐级电离能如下表:
电离能/KJ/mol | I1 | I2 | I 3 | I4 |
Mn | 717.3 | 1509.0 | 3248 | 4940 |
Fe | 762.5 | 1561.9 | 2957 | 5290 |
Co | 760.4 | 1648 | 3232 | 4950 |
铁元素的第三电离能明显低于锰元素和钴元素,其原因是____。
③实验室可用赤血盐K3[Fe(CN)6]检验Fe2+离子,在赤血盐中铁元素的化合价为____,中心离子的配位数为______。
(2)利用反应:X+C2H2+NH3→Cu2C2+NH4Cl(未配平)可检验乙炔。
①化合物X晶胞结构如图,据此可知X的化学式为_______。

②乙炔分子中σ键与π键数目之比为______,碳原子的杂化方式为_______;NH4+空间构型为______(用文字描述)。
(3)①下列三种化合物a.AlCl3 b.NaCl c.Al2O3沸点由高到低依次是_______(填编号),其原因是____________。
②Al单质中原子采取面心立方最密堆积,其晶胞边长为0.405nm,列式表示Al单质的密度_______g/cm3(不必计算出结果)。