题目内容
【题目】按要求填空
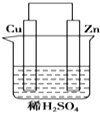
(1)按如图电解氯化钠的稀溶液可制得漂白液,写出该电解池中发生反应的总反应方程式:; 
(2)将充分电解后所得溶液逐滴加入到酚酞试液中,观察到的现象是 .
【答案】
(1)NaCl+H2O ![]() NaClO+H2↑
NaClO+H2↑
(2)溶液变红后褪色
【解析】解:(1)电解饱和氯化钠溶液,反应的方程式为:2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑,同时发生反应Cl2+2NaOH=NaCl+NaClO+H2O,故该电解池中发生反应的总反应方程式为:NaCl+H2O
2NaOH+Cl2↑+H2↑,同时发生反应Cl2+2NaOH=NaCl+NaClO+H2O,故该电解池中发生反应的总反应方程式为:NaCl+H2O ![]() NaClO+H2↑,
NaClO+H2↑,
所以答案是:NaCl+H2O ![]() NaClO+H2↑;(2)电解后得到NaClO溶液,显碱性,且具有强氧化性,滴入酚酞溶液中,观察到溶液变红后褪色,
NaClO+H2↑;(2)电解后得到NaClO溶液,显碱性,且具有强氧化性,滴入酚酞溶液中,观察到溶液变红后褪色,
所以答案是:溶液变红后褪色.

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】氮元素的化合物种类繁多,性质也各不相同.
(1)图1为一定温度下1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图.已知E1=147.5kJmol﹣1 , E2=376.2kJmol﹣1(E1、E2为反应的活化能).若在反应体系中加入催化剂,反应速率增大,则E1(填“增大”、“减小”或“不变”).该反应的热化学方程式为 . 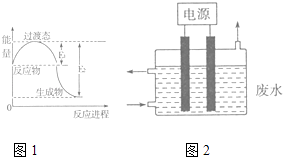
(2)硝基苯甲酸乙酯在OH﹣存在的条件下发生水解反应:
O2NC6H4COOC2H5+OH﹣O2NC6H4COOO﹣+C2H5OH
两种反应物的初始浓度均为0.050molL﹣1 , 某温度下测得O2NC6H4COOC2H5的转化率α随时间变化的数据如下表所示:
t/s | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
α/% | 0 | 33 | 42 | 49 | 59 | 73 | 74 | 75 | 75 |
回答下列问题:①该反应在330s~530s的平均反应速率为(只列算式,不做运算)
②为提高O2NC6H4COOC2H5的转化率,可以采取的措施有 . (写1条即可)
(3)2015年8月12日天津港爆炸中有一定量的氰化物泄露,可用如图2所示装置除去含CN﹣、Cl﹣废水中的CN﹣ , 控制溶液pH为9~10,阳极产生的ClO﹣将CN﹣氧化为两种无污染的气体,该反应的离子方程式为 , 其中两个电极的材料分别为石墨和铁,则石墨作极,其电极反应式为 .