题目内容
【题目】一瓶不纯的K2CO3粉末,所含杂质可能是KNO3、Ca(NO3)2、KCl、CuCl2、Na2SO4中的一种或几种。为确定其成分,进行如下实验:
(1)取少量该粉末于烧杯中,加入适量蒸馏水,充分搅拌,得无色澄清溶液。
(2)在上述无色溶液中加入足量的BaCl2溶液,有白色沉淀生成,过滤,得无色溶液。
(3)取少许(2)中过滤后的无色溶液于试管中,滴加AgNO3溶液有白色沉淀生成。
下列说法正确的是( )
A.杂质中可能含有KNO3、CuCl2
B.杂质中肯定不含有Ca(NO3)2、CuCl2
C.杂质中肯定含有KCl、Na2SO4
D.杂质中肯定含有KCl,可能含有KNO3、Na2SO4
【答案】B
【解析】
(1)溶液呈无色澄清,说明溶液中一定不含有Cu2+,因溶液中一定含有![]() ,则一定不含有Ca2+;
,则一定不含有Ca2+;
(2)加入BaCl2溶液产生白色沉淀,该沉淀中一定有BaCO3,可能含有BaSO4,样品中可能含有Na2SO4;
(3)加入AgNO3溶液有白色沉淀生成,该白色沉淀为AgCl,但在(2)步中加入了Cl-,因此无法确定样品中是否含有KCl;
根据上述分析可知,样品中一定不含Ca(NO3)2、CuCl2,无法确定含有KNO3、KCl、Na2SO4,故答案为B。

 名校课堂系列答案
名校课堂系列答案【题目】由下列实验及现象不能得出相应结论的是( )
实验 | 现象 | 结论 | |
A | 向浓度均为 |
| 非金属性: |
B. | 向含有酚酞的 | 观察到红色变浅 | 证明 |
C | 室温下,用pH试纸测 |
|
|
D. | 向盛有10滴 | 有黄色沉淀生成 |
|
A.AB.BC.CD.D
【题目】钴酸锂(LiCoO2)电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
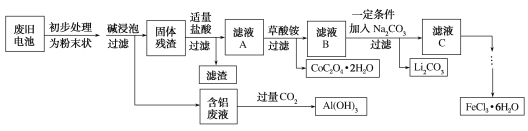
已知:①还原性:Cl->Co2+;
②Fe3+和![]() 结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
(1)废旧电池初步处理为粉末状的目的是________。
(2)从含铝废液得到Al(OH)3的离子方程式为___________
(3)滤液A中的溶质除HCl、LiCl外还有________(填化学式)。写出LiCoO2和盐酸反应的化学方程式____________
(4)滤渣的主要成分为_______(填化学式)。
(5)在空气中加热一定质量的CoC2O4·2H2O固体样品时,其固体失重率数据见下表,请补充完整表中问题。
已知:①CoC2O4在空气中加热时的气体产物为CO2。
②固体失重率=对应温度下样品失重的质量/样品的初始质量。
序号 | 温度范围/℃ | 化学方程式 | 固体失重率 |
Ⅰ | 120~220 | CoC2O4·2H2O CoC2O4+2H2O | 19.67% |
Ⅱ | 300~350 | ______ | 59.02% |
(6)已知Li2CO3的溶度积常数Ksp=8.64×10-4,将浓度为0.02 mol·L-1的Li2SO4和浓度为0.02 mol·L-1的Na2CO3溶液等体积混合,则溶液中的Li+浓度为________ mol·L-1。