题目内容
11.中学化学实验中,用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和热的测定.如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量不相等(填“相等、不相等”),所求中和热相等(填“相等、不相等”)分析 反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念是强酸和强碱反应生成1mol水时放出的热来回答.
解答 解:反应放出的热量和所用酸以及碱的量的多少有关,并若用60mL 0.50mol/L 盐酸跟50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,中和热数值相等,
故答案为:不相等;相等.
点评 本题考查学生有关中和热的测定知识,注意中和热与酸、碱的物质的量无关,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
1.反应:
①N2O5(g)?N2O3(g)+O2(g)
②N2O3(g)?N2O(g)+O2(g)
在0.5L密闭容器中,将2.5mol N2O5加热气化,并按上述①②两式分解,在某温度下达到平衡,测得O2的平衡浓度为4.4mol•L-1,N2O3的平衡浓度为1.6mol•L-1,
则下列各项判断正确的是( )
①N2O5(g)?N2O3(g)+O2(g)
②N2O3(g)?N2O(g)+O2(g)
在0.5L密闭容器中,将2.5mol N2O5加热气化,并按上述①②两式分解,在某温度下达到平衡,测得O2的平衡浓度为4.4mol•L-1,N2O3的平衡浓度为1.6mol•L-1,
则下列各项判断正确的是( )
| A. | N2O5的平衡浓度为3.0mol•L-1 | B. | N2O5的转化率为80% | ||
| C. | N2O的平衡浓度为4.4mol•L-1 | D. | N2O的平衡浓度为1.4mol•L-1 |
2.下列气体的排放不会造成酸雨的是( )
| A. | SO2 | B. | NO | C. | NO2 | D. | CO2 |
19.近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取.以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为:KI+3H2O═KIO3+3H2↑.下列有关说法正确的是( )
| A. | 电解时,石墨作阴极,不锈钢作阳极 | |
| B. | 电解时,阳极反应是:I--6e-+3H2O═IO3-+6H+ | |
| C. | 溶液调节至强酸性,对生产有利 | |
| D. | 电解时溶液中I-向阴极迁移 |
6.下列化合物的1H-NMR谱图中吸收峰数目正确的是( )
| A. | CH3CH2CH2CH3(3组) | B. | CH2═CH-CH2CH3(2组) | ||
| C. | 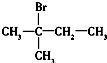 (4组) (4组) | D. | 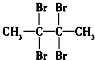 (1组) (1组) |
16.实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
| A. | 950mL 111.2g | B. | 500mL 117g | ||
| C. | 1 000mL 117g | D. | 任意规格 111.2g |
3.以下关于化学实验中“先与后”的说法中正确的是( )
①加热试管时,先均匀加热,后局部加热
②用排水法收集气体后,先移出导管后撤酒精灯
③制取气体时,先检验装置气密性后装药品
④点燃可燃性气体(如H2、CO等)时,先检验气体纯度后点燃
⑤做H2还原CuO实验时,先通H2后加热CuO,反应完毕后,先撤酒精灯待试管冷却后停止通H2.
①加热试管时,先均匀加热,后局部加热
②用排水法收集气体后,先移出导管后撤酒精灯
③制取气体时,先检验装置气密性后装药品
④点燃可燃性气体(如H2、CO等)时,先检验气体纯度后点燃
⑤做H2还原CuO实验时,先通H2后加热CuO,反应完毕后,先撤酒精灯待试管冷却后停止通H2.
| A. | ①②③⑤ | B. | ①②④⑤ | C. | ①②③④ | D. | 全部 |
20.火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2→Cu2S+2FeS+SO2,下列说法正确的是( )
| A. | 每转移l.2 mol电子,有0.2mol硫被氧化 | |
| B. | CuFeS2仅作还原剂,硫元素被氧化 | |
| C. | 每生成1molCu2S,有4mol硫被氧化 | |
| D. | SO2只是氧化产物 |
1.某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO.其过程如:mCeO2$→_{①}^{太阳能}$(m-x)CeO2•xCe+xO2,(m-x)CeO2•xCe+xH2O+xCO2$→_{②}^{900℃}$mCeO2+xH2+xCO.下列说法不正确的是( )
| A. | 该过程中CeO2需要不断补充 | |
| B. | 该过程实现了太阳能向化学能的转化 | |
| C. | 二氧化铈(CeO2)是该反应的催化剂 | |
| D. | 该反应的副产物是O2 |