题目内容
10.下列说法中正确的是( )| A. | 凡是放热反应都是自发的,吸热反应都是非自发的 | |
| B. | 自发反应一定是熵增大,非自发反应一定是熵减小或不变 | |
| C. | 醋酸溶液的导电能力可能比稀硫酸强 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H不同 |
分析 A、根据自发反应的判断依据判断,判断依据为:△G=△H-T△S,当△G=△H-T△S<0,反应能自发进行;当△G=△H-T△S=0,反应达到平衡状态;当△G=△H-T△S>0,反应不能自发进行;
B、熵增的反应不一定自发,熵减的反应不一定非自发;
C、溶液的导电能力取决于溶液中离子浓度大小;
D、反应热△H的大小取决于反应物和生成物的总能量的相对大小.
解答 解:A、化学反应能否自发进行的判断依据为:△G=△H-T△S,当△G=△H-T△S<0,反应能自发进行;当△G=△H-T△S=0,反应达到平衡状态;当△G=△H-T△S>0,反应不能自发进行,故放热反应不一定自发,吸热反应不一定非自发,故A错误;
B、熵增的反应不一定自发,自发反应不一定是熵增的反应,熵减的反应不一定非自发,非自发的反应不一定是熵减或不变的反应,故B错误;
C、溶液的导电能力取决于溶液中离子浓度大小,与电解质的强弱无关,故醋酸溶液的导电能力可能比稀硫酸强,故C正确;
D、反应热△H的大小取决于反应物和生成物的总能量的相对大小,与反应条件无关,故无论是点燃还是光照,对反应热无影响,故D错误.
故选C.
点评 本题考查了反应的熵变与反应能否自发的关系以及反应热的决定因素,应注意的是反应热△H的大小取决于反应物和生成物的总能量的相对大小,与反应条件无关.

练习册系列答案
相关题目
5.下列有关化学用语表示正确的是( )
| A. | 过氧化钠的电子式: | |
| B. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子的结构示意图: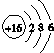 | |
| D. | 福尔马林可作食品的保鲜剂 |
3.下列各组化合物中,化学键类型完全相同的是( )
| A. | CaCl2 和 NaHS | B. | Na2O 和Na2O2 | C. | CO2 和HCl | D. | Na2O2 和NaOH |
5.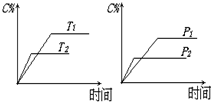 可逆反应mA(固)+nB(气)?e C(气)+f D(气)△H,反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图:下列叙述正确的是( )
可逆反应mA(固)+nB(气)?e C(气)+f D(气)△H,反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图:下列叙述正确的是( )
 可逆反应mA(固)+nB(气)?e C(气)+f D(气)△H,反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图:下列叙述正确的是( )
可逆反应mA(固)+nB(气)?e C(气)+f D(气)△H,反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图:下列叙述正确的是( )| A. | 达平衡后,加入催化剂则C%增大 | |
| B. | 达平衡后,增加A的量有利于平衡向右移动 | |
| C. | 化学方程式中n>e+f | |
| D. | 达平衡后升温,则平衡向左移动,且△H<0 |
1.已知AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$,常温下,在AG=-10的溶液中能大量存在的离子组是( )
| A. | Cl-,AlO2-,SO32-,Na+ | B. | NO3-,CH3COO-,Na+,NH4+ | ||
| C. | Cl-,NO3-,Mg2+,K+ | D. | SO42-,HCO3-,Cl-,K+ |
18.无法判断可逆反应2SO2(g)+O2(g)?2SO3(g)是否达到平衡的理由是( )
| A. | 气体的浓度不再变化 | B. | 容器内压强不再改变 | ||
| C. | 气体的分子数不再变化 | D. | 各气体的浓度相等 |
19.0.25mol Ca(OH)2跟0.3mol H3PO4在一定条件下充分反应,得到CaHPO4和Ca(H2PO4)2,则这两种产物的物质的量之比为( )
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 4:1 |