题目内容
【题目】研究金属与硝酸的反应,实验如下。
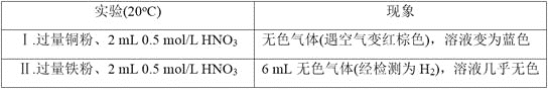
(1)Ⅰ中的无色气体是_________。
(2)Ⅱ中生成H2的离子方程式是______________________________________。
(3)研究Ⅱ中的氧化剂
①甲同学认为该浓度的硝酸中H+的氧化性大于NO3-,所以NO3-没有发生反应。乙同学依据Ⅰ和Ⅱ证明了甲的说法不正确,其实验证据是_______________________________。
②乙同学通过分析,推测出NO3-也能被还原,依据是___________________________,进而他通过实验证实该溶液中含有NH4+,其实验操作是__________________________
(4)根据实验,金属与硝酸反应时,影响硝酸还原产物不同的因素有_________________________试推测还可能有哪些因素影响_________(列举1条)。
【答案】NO或一氧化氮 Fe+2H+===Fe2++H2↑ 硝酸浓度相同,铜的还原性弱于铁,但Ⅰ中溶液变蓝,同时没有氢气放出 NO3- 中氮元素的化合价为最高价,具有氧化性 取Ⅱ中反应后的溶液,加入足量NaOH溶液并加热,产生有刺激性气味并能使湿润红色石蕊试纸变蓝的气体 金属的种类、硝酸的浓度 温度
【解析】
(1)铜与硝酸反应生成无色气体,该气体与空气变红,故该气体是NO;
(2)Ⅱ中铁与硝酸溶液中的H+发生氧化还原反应生成H2;
(3)①如果硝酸根离子没有发生反应,则Ⅰ溶液不会变蓝,溶液变蓝说明铜被氧化为铜离子;
②元素化合价处于最高价,具有氧化性,NH4+的检验可以与浓的氢氧化钠溶液在加热的条件下反应,产生的气体通过湿润的红色石蕊试纸来检验;
(4)金属与硝酸反应时,影响硝酸还原产物不同的因素是金属活泼性、硝酸的浓度、温度。
(1)铜与硝酸反应生成无色气体,该气体与空气变为红棕色,故该气体为NO,红棕色的气体为NO2;
(2)Ⅱ中铁与硝酸溶液中的H+发生氧化还原反应生成H2,离子反应方程式为:Fe+2H+=Fe2++H2↑;
(3)①如果硝酸根离子没有发生反应,则Ⅰ溶液不会变蓝,溶液变蓝说明铜被氧化为铜离子,其实验证据是硝酸浓度相同,铜的还原性比铁的还原性弱,但Ⅰ中溶液变蓝,同时没有氢气放出;
②元素化合价处于最高价,具有氧化性,NO3-中氮元素的化合价为最高价,具有氧化性,被还原;
NH4+的检验可以与浓的氢氧化钠溶液在加热的条件下反应,产生的气体通过湿润的红色石蕊试纸来检验,具体操作为:取Ⅱ中反应后的溶液,加入足量NaOH溶液并加热,产生有刺激性气味并能使湿润红色石蕊试纸变蓝的气体;
(4)金属与硝酸反应时,影响硝酸还原产物不同的因素是金属活泼性、硝酸的浓度、温度。

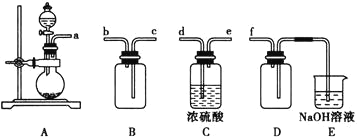
【题目】某探究性学习小组设计如图所示装置分别进行如下探究实验,请回答下列问题:
实验 | 药品 | 制取气体 | 量气管中的液体 |
Ⅰ | Cu、稀HNO3 | H2O | |
Ⅱ | Na OH固体、浓氨水 | NH3 | |
Ⅲ | 镁铝合金、足量NaOH溶液 | H2 | H2O |
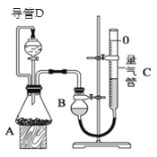
(1)实验I通过收集并测量NO气体的体积来探究铜样品的纯度,有的同学认为该实验设计不可行,主要原因是__________________________;
(2)实验Ⅱ中量气管中的液体最好是_______(填字母编号,下同)
A.NaOH溶液B.氨水C.煤油D.氯化铵溶液
实验剩余的NH3需吸收处理,以下各种尾气吸收装置中,不能防止倒吸的是________;
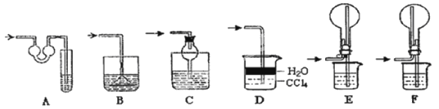
(3)①写出实验Ⅲ中涉及的离子反应方程式_________________________;
②反应前,先对量气管进行第一次读数。读数时,应注意的操作是________________,并使视线与凹液面最低处相平;反应后,待装置温度冷却到室温时,再对量气管进行第二次读数。
③实验Ⅲ在25℃、1.01×105Pa条件下获得以下数据:
编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
① | 1.0g | 10.0mL | 376.6mL |
② | 1.0g | 10.0mL | 364.7mL |
③ | 1.0g | 10.0mL | 377.0mL |
根据上述数据,计算出镁铝合金中铝的质量分数为_______________。