��Ŀ����
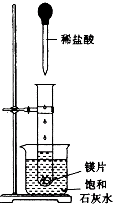
����Ŀ��Ϊ���о���ѧ��ӦA��B===C��D�������仯�����ijͬѧ�������ͼ��ʾװ�á�����ʢ��A���Թ��еμ��Լ�Bʱ������U�ι��м״�Һ���½��Ҵ�Һ���������Իش��������⣺

��1���÷�ӦΪ____________(��������������������)��Ӧ��
��2��A��B����������C��D��������____________(����������������)��
��3�������еĻ�ѧ��ͨ��________ת����________�ͷų�����
��4����Ӧ�ﻯѧ���������յ�����________(����������������)�������ﻯѧ���γɷų���������
��5��д��һ���������������Ļ�ѧ����ʽ��________________________________��
���𰸡� ���� �� ��ѧ��Ӧ ���� �� 2Al��6HCl=2AlCl3��3H2��(��2Na��2H2O=2NaOH��H2����NaOH��HCl=NaCl��H2O�Ⱥ����𰸾���)
��������������Ҫ���黯ѧ��Ӧ�е������仯��
��1�������������ͣ������÷�ӦΪ���ȷ�Ӧ��
��2�����ȷ�Ӧ��Ӧ��������������������������������A��B����������C��D������������
��3�������еĻ�ѧ��ͨ����ѧ��Ӧת���������ͷų�����
��4���÷�Ӧ����H=��Ӧ�ﻯѧ���������յ�����-�����ﻯѧ���γɷų�������<0�����Է�Ӧ�ﻯѧ���������յ��������������ﻯѧ���γɷų���������
��5�����������������Ƿ��ȷ�Ӧ�Ļ�ѧ����ʽ��2Al��6HCl=2AlCl3��3H2��(��2Na��2H2O=2NaOH��H2����NaOH��HCl=NaCl��H2O�Ⱥ����𰸾���)��