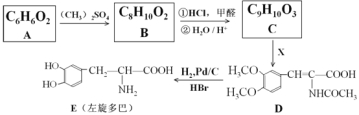
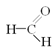
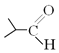
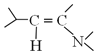
题目内容
【题目】下列有关电解质溶液的说法正确的是( )
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中 减小
减小
B.将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C.在pH=8的NaB溶液中:c(Na+)-c(B-)=9.9×10-8mol·L-1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
【答案】D
【解析】
A、加水促进醋酸的电离;B、水解常数只受温度影响,升高温度水解平衡正向移动;C、根据电荷守恒分析;D、AgCl、AgBr的饱和溶液中存在AgCl(s)+Br-AgBr(s)+Cl-,该反应的平衡常数K=![]() 。
。
A、向0.1molL-1CH3COOH溶液中加入少量水,溶液中c(CH3COO-)减小,由于温度不变Ka(CH3COOH)不变,根据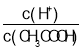 ×c(CH3COO-)=Ka(CH3COOH)可知,
×c(CH3COO-)=Ka(CH3COOH)可知,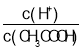 的比值增大,故A错误;
的比值增大,故A错误;
B、CH3COO-的水解为吸热反应,将CH3COONa溶液从20℃升温至30℃,CH3COO-的水解程度增大,则水解平衡常数Kh(CH3COO-)增大,所以![]() =
=![]() 的比值减小,故B错误;
的比值减小,故B错误;
C、常温下在pH=8的NaB溶液中,c(H+)=1×10-8molL-1,c(OH-)=1×10-6molL-1,根据电荷守恒可知:c(Na+)-c(B-)=c(OH-)-c(H+)=9.9×10-7molL-1,故C错误;
D、AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中银离子浓度相同,温度不变,溶度积常数不变,则溶液中![]() =
=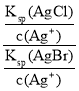 =
= ![]() 的比值不变,故D正确。
的比值不变,故D正确。
答案选D。

【题目】(1)Al2(SO4)3溶液加热蒸干并灼烧最终得到物质是________________(填化学式),将NaHCO3与Al2(SO4)3两者溶液混合后可做泡沫灭火剂,其原理是_____________________(用离子方程式表示)
(2)实验室溶液中常用NaOH来进行洗气和提纯。当100mL 1mol·L-1的NaOH溶液吸收标准状况下2.24LSO2时,所得溶液中各离子浓度由大到小的顺序为____________________________
(3)25℃时,几种离子开始沉淀时的pH如下表:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加NaOH溶液时,_____先沉淀(填离子符号),要使0.3mol·L-1硫酸铜溶液中Cu2+沉淀较为完全(当Cu2+浓度降至10-5 mol·L-1时),则应向溶液里加入氢氧化钠溶液使溶液pH为____(KspCu(OH)2=1×10-20)
【题目】中国传统文化中包括许多科技知识。下列古语中不涉及化学变化的是
千淘万漉虽辛苦,吹尽狂沙始到金 |
熬胆矾(CuSO4·5H2O) 铁釜,久之亦化为铜 |
凡石灰(CaCO3), 经火焚炼为用 |
丹砂(HgS)烧之成水银,积变又成丹砂 |
A | B | C | D |
A. A B. B C. C D. D