题目内容
【题目】关于下列各装置图的叙述中,不正确的是![]()
![]()

A.用装置①电解氯化铜溶液,则a为阳极,发生氧化反应
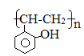
B.装置②为原电池,总反应是:![]()
C.图③所示柱形图,纵坐标表示第二周期元素最高正价随原子序数的变化
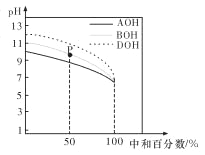
D.图④所示曲线,表示该反应是放热反应
【答案】C
【解析】
A.电流流出的一极为正极,与正极相连的为阳极,则a与正极相连,为阳极,阳极上阴离子失电子发生氧化反应,故A正确;
B.Fe、Cu、氯化铁溶液形成的原电池中,Fe为负极,电池总反应为Fe与铁离子之间的反应,则总反应是:![]() ,故B正确;
,故B正确;
C.第二周期元素中O、F元素无正价,而图中O、F分别为![]() 、
、![]() 价,故C错误;
价,故C错误;
D.图![]() 中反应物的总能量大于生成物的总能量,该反应为放热反应,故D正确。
中反应物的总能量大于生成物的总能量,该反应为放热反应,故D正确。
故选:C。

练习册系列答案
相关题目
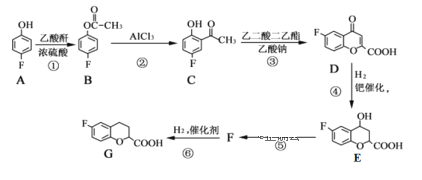
【题目】某工厂对制革工业污泥中铬的处理工艺流程如下:

已知硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)酸浸时,为了提高浸取率可采取的措施有_________、___________。(答出两点)。
(2)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 | — | — |
沉淀完全时的pH | 3.7 | 5.4(>8溶解) | 9(>9溶解) |
①用NaOH调节溶液的pH不能超过8,其理由是________________________________。
②常温下,当pH=8时,Mg2+是否开始沉淀(溶液中镁离子浓度不超过1mol·L-1)___________ 。 (填“是”或“否”)若要使Mg2+完全沉淀,溶液的pH至少为_________(已知Ksp[Mg(OH)2]=1. 6×10-12,lg2=0.3)。