题目内容
 某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.请填写下列空白:
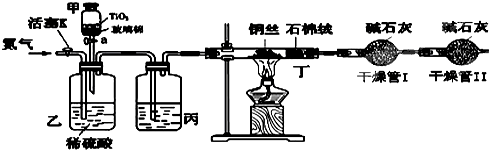
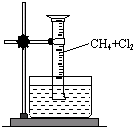
【实验一】用如图所示装置,收集一试管甲烷和氯气的混合气体,照后观察到量筒内形成一段水柱,认为有氯化氢生成.
(1)该反应的反应类型为
(2)该反应的化学方程式为
(3)水槽中盛放的液体应为
A.水 B.饱和石灰水 C.饱和食盐水 D.饱和NaHCO3溶液
【实验二】收集一试管甲烷和氯气的混合气体,光照反应后,滴加AgNO3溶液,看到有白色沉淀生成,认为有氯化氢生成.
(4)该实验设计的错误之处
(5)写出碳原子数为9的甲烷的一种同系物的名称,已知它的一氯代物有两种:
(2)甲烷与氯气在光照条件下能够发生取代反应,第一步反应为甲烷中1个H被氯原子取代生成一氯甲烷,据此写出反应的化学方程式;
(3)水槽中的液体必须满足:氯气在该溶液中溶解度很小,以便证明氯气与甲烷发生了反应;
(4)氯水中含有氯离子,加入硝酸银溶液同样产生氯化银沉淀,干扰了氯离子的检验;
(5)该烷烃的一氯代物有两种,说明其分子中含有的氢原子有两种,据此写出满足条件的壬烷的同分异构体.
故答案为:取代反应;
(2)甲烷中一个氢原子被氯气取代的反应方程式为:CH4+Cl2
| 光照 |
故答案为:CH4+Cl2
| 光照 |
(3)Cl2+H2O?H++Cl-+HClO,氯气在饱和氯化钠溶液中的溶解度较小,所以防止氯气和水反应,水槽中盛放的液体最好为饱和食盐水;由于氯气在水中溶解度较大、氯水能够与饱和石灰水、饱和碳酸氢钠溶液反应,干扰的实验结果,而不能使用水,更不能使用饱和石灰水、饱和碳酸氢钠溶液,
故答案为:C;
(4)氯水中存在化学平衡:Cl2+H2O?H++Cl-+HClO;次氯酸是弱电解质,溶液中存在三种分子:Cl2、HClO、H2O;四种离子:H+、Cl-、ClO-、OH-(少量),所以当氯水中加入AgNO3溶液时会发生反应:Ag++Cl-=AgCl↓,同样会产生白色沉淀,干扰了氯离子的检验,
故答案为:氯水中加入AgNO3溶液也会产生白色沉淀;
(5)碳原子数为9的烷烃为壬烷,庚烷中一氯代物有两种,说明该壬的同分异构体中,含有的氢原子种类只有两种,联系乙基的一氯代物只有一种,用四个乙基将甲烷中四个氢原子取代就可以得到壬烷,且其一氯代物只有两种,该壬烷的结构简式为:CH3CH2C(CH2CH3)2CH2CH3,该有机物的名称为:3,3-二甲基戊烷,
故答案为:3,3-二乙基戊烷.

研究氧化还应常用到高锰酸钾,高锰酸钾是一种重要的化学试剂。为了增强其氧化性常将其酸化,但在酸性条件下其水溶液不很稳定,会分解生成二氧化锰和氧气,而在中性或弱碱性溶液中分解速度很慢,见光分解速度加快。
(1)高锰酸钾溶液保存的注意事项______________________________________________。
酸性溶液中高锰酸钾分解的离子方程式 _______________________________________。
(2)草酸可使酸性高锰酸钾溶掖褪色,请写出此反应的离子方程式______________________。
(3)某学习小组为了探究高锰酸钾溶液和草酸钠溶液的反应过程,将高锰酸钾溶液逐滴地滴入一定体积的酸性草酸钠溶液中(温度相同,并不断振荡时),记录的现象如下表:
|
滴入 KMnO4 认溶液的次序(每滴溶液等体积) |
KMnO4 溶液紫色褪去的时间 |
|
先滴入第 1 滴 |
1min |
|
褪色后再滴入第 2 滴 |
15s |
|
褪色后再滴入第 3 滴 |
3s |
|
褪色后再滴入第 4 滴 |
1s |
请分析高锰酸钾溶液褪色时间变化的原因________________________________________。
(4)该学习小组在获取了上述经验和结论以后,用稳定的物质草酸钠来标定高锰酸钾济液的浓度。他们准确称取2.680g纯净的草酸钠配成500mL溶液,每次准确量取25.00mL溶液酸化后用KMnO4 溶液滴定。
①高锰酸钾溶液应装在______(填下途中的仪器编号)。
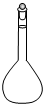
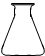

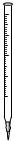
甲 乙 丙 丁
②为了防止高锰酸钾在酸性条件下分解而造成误差,滴定开始时,操作上必须是______________。
③当溶液呈微红色且半分钟内不褪色,消耗KMnO4溶液20.00mL(多次测定的平均值),则KMnO4溶液的浓度为________________。
(附原子相对质量K=39Mn=55O=16 Na=23C=12)
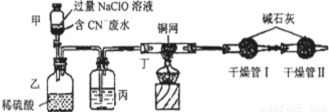
 (2013?资阳二模)某消毒液的主要成分为NaCl和NaClO,在空气中易吸收CO2而变质,且NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O.某学习小组拟探究该消毒液的变质情况.
(2013?资阳二模)某消毒液的主要成分为NaCl和NaClO,在空气中易吸收CO2而变质,且NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O.某学习小组拟探究该消毒液的变质情况.