题目内容
20.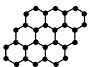 金刚石晶体结构中,每个碳原子与周围四个碳原子形成正四面体空间立体网状结构,则金刚石晶体中碳原子数与共价键之比是( )
金刚石晶体结构中,每个碳原子与周围四个碳原子形成正四面体空间立体网状结构,则金刚石晶体中碳原子数与共价键之比是( )| A. | 1:2 | B. | 2:1 | C. | 1:4 | D. | 4:1 |
分析 金刚石晶体中每个C原子处于其他4个C原子构成的正四面体的内部,向周围无限延伸形成空间立体网状结构,最小的环是立体六元环,每个C原子周围有4条共价键,而每2个碳原子形成1个共价键,据此计算解答.
解答 解:金刚石晶体中每个C原子处于其他4个C原子构成的正四面体的内部,向周围无限延伸形成空间立体网状结构,最小的环是立体六元环,每个C原子周围有4条共价键,而每2个碳原子形成1个共价键,所以金刚石晶体中C原子数与C-C键数之比为1:2,
故选:A.
点评 本题考查了物质的结构,熟悉金刚石晶体结构特点是解题关键,题目难度不大.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
7.下列叙述正确的是( )
| A. | 1molH2O的质量为18g•mol-1 | |
| B. | CH4的摩尔质量为16g | |
| C. | 3.01×1023个SO2分子的质量为32 g | |
| D. | 1mol任何物质均含有6.02×1023个分子 |
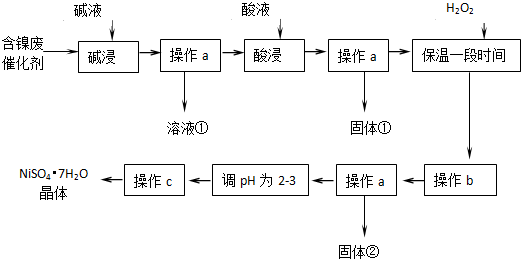
8.某化学小组通过査阅资料,设计了如图所示的方法以含镍催化剂为原料来制备NiSO4•7H20.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).
部分阳离子以氢氧化物形式沉淀时的pH如下:
(1)“碱浸”时反应的离子方程式是2Al+2OH-+2H2O═2AlO2-+3H2↑、Al2O3+2OH-═2AlO2-+H2O.
(2)“酸浸”时所加入的酸是H2SO4(填化学式).
(3)加入H2O2时发生反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2-7.1.
(5)NiS04•7H20可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M═NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.

部分阳离子以氢氧化物形式沉淀时的pH如下:
| 沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
(2)“酸浸”时所加入的酸是H2SO4(填化学式).
(3)加入H2O2时发生反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2-7.1.
(5)NiS04•7H20可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M═NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.
5.下列烷烃的命名错误的是( )
| A. | 3-甲基丁烷 | B. | 2-甲基-3-乙基戊烷 | ||
| C. | 2,2-二甲基丁烷 | D. | 2,3-二甲基丁烷 |
 ;在上述由SiCl4气体制纯硅的反应中,测得每生成1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:SiCl4(g)+2H2(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g);△H=+0.025akJ•mol-1.
;在上述由SiCl4气体制纯硅的反应中,测得每生成1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:SiCl4(g)+2H2(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g);△H=+0.025akJ•mol-1.

 中和热是指酸跟碱发生中和反应生成l mol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:
中和热是指酸跟碱发生中和反应生成l mol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题: