题目内容
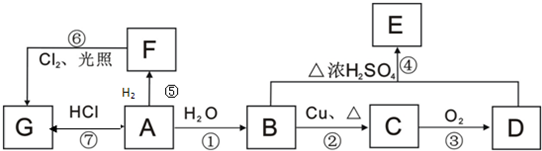
9.对如图所示实验装置的说明错误的是( )| A. |  能作为SO2的干燥装置 | |
| B. |  验证铁钉的吸氧腐蚀 | |
| C. |  可用于测量Cu与浓硝酸反应生成NO2的体积 | |
| D. |  可证明酸性:H2SO4>H2CO3>H2SiO3 |
分析 A.二氧化硫可用浓硫酸干燥;
B.如发生吸氧腐蚀,可观察到导管液面上升;
C.二氧化氮不能用排水法收集;
D.硫酸酸性比碳酸强,与碳酸钠反应生成二氧化碳气体,碳酸比硅酸的酸性强,二氧化碳与硅酸钠溶液反应生成硅酸沉淀.
解答 解:A.二氧化硫可用浓硫酸干燥,干燥时气体从长导管进,故A正确;
B.如发生吸氧腐蚀,试管内压强减小,可观察到导管液面上升,故B正确;
C.二氧化氮与水反应生成硝酸和NO,不能用排水法收集,故C错误;
D.硫酸酸性比碳酸强,与碳酸钠反应生成二氧化碳气体,碳酸比硅酸的酸性强,二氧化碳与硅酸钠溶液反应生成硅酸沉淀,可用于比较酸性强弱,故D正确.
故选C.
点评 本题考查较为综合,涉及除杂、气体的收集、金属的 腐蚀以及酸性的比较等知识,为高考常见题型,侧重于学生的分析、实验能力的考查,注意把握实验的严密性、可行性的评价,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.苯环结构中不存在C-C单键和C=C双键的交替结构,可以作为证据的事实( )
①苯不能使酸性KMnO4溶液褪色;
②苯环中碳碳键的键长均相等;
③苯能在催化剂存在和加热的条件下氢化生成环己烷;
④邻二甲苯只有一种结构;
⑤苯在FeBr3存在下同液溴发生取代反应,但不因化学反应而使溴水褪色.
①苯不能使酸性KMnO4溶液褪色;
②苯环中碳碳键的键长均相等;
③苯能在催化剂存在和加热的条件下氢化生成环己烷;
④邻二甲苯只有一种结构;
⑤苯在FeBr3存在下同液溴发生取代反应,但不因化学反应而使溴水褪色.
| A. | ②③④⑤ | B. | ①③④⑤ | C. | ①②④⑤ | D. | ①②③④ |
10.某学生为了完成一个家庭小实验,自制烷烃的分子模型,对于CnH2n+2的烷烃,做球棍模型时,除需做3n+2个球外还需要的棍(共价键)数为( )
| A. | 3n+2 | B. | 3n+1 | C. | 3n | D. | 3n-1 |
4.生产生活中处处有化学,下列有关说法错误的是( )
| A. | 铁表面镀锌可增强铁的抗腐蚀性 | |
| B. | 糖类、油脂、蛋白质等是食物中的基本营养物质 | |
| C. | 雾霾、温室效应、光化学烟雾的形成都与氮的氧化物有关 | |
| D. | 氯气和活性炭是常用的漂白剂,但同时使用会降低或失去漂白性 |
14.化学知识在生产、生活中有着广泛的应用.下列说法中正确的是( )
| A. | 铅蓄电池属于二次电池 | |
| B. | 氢氟酸可用于蚀刻玻璃是因为其具有强酸性 | |
| C. | 为了防止食品受潮,常在食品包装袋中放入活性铁粉 | |
| D. | 用于制光缆的光导纤维是新型有机高分子材料 |
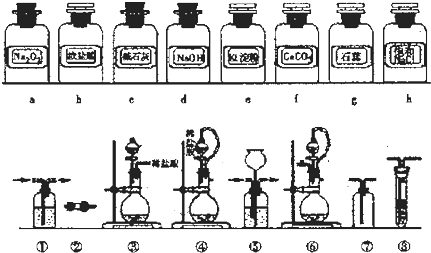
1.实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气.某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气,供选用的实验试剂及装置如下(部分导管、蒸馏水略去).
I.写出制取氯气的化学方程式或离子方程式:
①MnO2与浓盐酸制取氯气的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
②Na2 O2与浓盐酸制备氯气的化学方程式Na2O2+4HCl=2NaCl+Cl2↑+2H2O.
Ⅱ.完成用Na2O2与浓盐酸制备氯气的有关问题:
(1)下列装置组合最合理的是D(填序号,需考虑实验结束撤除装置时残留有害气体的处理).
(2)尾气经处理后仍有较多气体排出,其主要原因用化学方程式表示为2Na2O2+2H2O=4NaOH+O2↑(或4Na2O2+4HCl=4NaCl+2H2O+O2↑)
(3)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①Na2O2能与水反应,会使原料的利用率降低,
②双氧水比Na2O2更经济.
(4)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一?否(填“是”或“否”);理由是产物不纯且难以分离.

I.写出制取氯气的化学方程式或离子方程式:
①MnO2与浓盐酸制取氯气的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
②Na2 O2与浓盐酸制备氯气的化学方程式Na2O2+4HCl=2NaCl+Cl2↑+2H2O.
Ⅱ.完成用Na2O2与浓盐酸制备氯气的有关问题:
(1)下列装置组合最合理的是D(填序号,需考虑实验结束撤除装置时残留有害气体的处理).
| 组合 | 制备装置 | 净化装置 | 检验装置/-试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ④⑥ | ⑤ | ⑧/g | ① |
(3)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①Na2O2能与水反应,会使原料的利用率降低,
②双氧水比Na2O2更经济.
(4)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一?否(填“是”或“否”);理由是产物不纯且难以分离.
18.下列溶液一定呈中性的是( )
| A. | pH=7的溶液 | |
| B. | c(H+)=c(OH-)的溶液 | |
| C. | 由强酸、强碱等物质的量反应得到的溶液 | |
| D. | 盐溶于水得到的溶液 |
19.用惰性电极电解下列足量的溶液,一段时间后,再加入一定量的另一物质(括号内)后,溶液能与原来溶液浓度一样的是( )
| A. | CuCl2(CuCl2溶液) | B. | AgNO3(Ag2O) | C. | NaCl(HCl溶液) | D. | CuSO4(Cu(OH)2) |