题目内容
【题目】(1)实验室在配制Cu(NO3)2的溶液时,常将Cu(NO3)2固体先溶于较浓的硝酸中,再用蒸馏水稀释到所需的浓度,其目的是____;
(2)FeCl3可用作净水剂,其原理是(用离子方程式表示)____;将Al2(SO4)3溶液蒸干,最后得到的主要固体物质是____(写化学式)。
(3)已知草酸是二元弱酸,常温下测得0.1mol/L的KHC2O4的pH为4.8,则此KHC2O4溶液中c(C2O42-)____c(H2C2O4)(填“大于”或“小于”或“等于”)。
(4)某小组同学探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。出现上述现象的原因是____(请用反应的离子方程式表示)。
【答案】抑制Cu2+的水解 Fe3++3H2O![]() Fe(OH)3(胶体)+3H+ Al2(SO4)3 大于 3ClO-+Al3++3H2O=3HClO+Al(OH)3↓
Fe(OH)3(胶体)+3H+ Al2(SO4)3 大于 3ClO-+Al3++3H2O=3HClO+Al(OH)3↓
【解析】
(1)Cu(NO3)2溶液中铜离子容易水解,在配制时,常将Cu(NO3)2固体先溶于较浓的硝酸中抑制Cu2+的水解;
故答案为 : 抑制Cu2+的水解;
(2)FeCl3可用作净水剂是因为Fe3+在水中易水解产生Fe(OH)3(胶体),Fe(OH)3(胶体)具有吸附作用;Al2(SO4)3溶液蒸干过程中因为Al3+水解后形成的Al(OH)3与H2SO4,而硫酸是难挥发性酸,加热时其浓度增大,又会与氢氧化铝反应生成Al2(SO4)3;
故答案为 Fe3++3H2O![]() Fe(OH)3(胶体)+3H+; Al2(SO4)3;
Fe(OH)3(胶体)+3H+; Al2(SO4)3;
(3)因为草酸氢钾为酸性,即证明草酸氢根离子的电离程度大于水解程度,所以电离的草酸氢根离子比水解的草酸氢根离子多,故c(C2O42-)>c(H2C2O4);
故答案为 >;
(4)NaClO和KAl(SO4)2溶液混合后,ClO-与Al3+会双水解生成氢氧化铝胶体,反应的离子方程式为3ClO-+Al3++3H2O=3HClO+Al(OH)3↓;
故答案为:3ClO-+Al3++3H2O=3HClO+Al(OH)3↓。

【题目】机动车排放的污染物主要有碳氢化合物、一氧化碳和氮氧化物等。
I.汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。
(1)已知: C(s)+O2(g) = CO2(g) △H1 = 393.5kJ·mol1
2C(s)+O2(g) = 2CO(g) △H2 = 221.0 kJ·mol1
N2(g)+O2(g) = 2NO(g) △H 3 =+180.5 kJ·mol1
CO和NO两种尾气在催化剂作用下生成N2的热化学方程式是_________________________。
(2)研究CO和NO的催化反应,用气体传感器测得在某温度下、一定体积的密闭容器中,不同时间NO和CO浓度如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(______)4mol·L1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)/(______)3mol·L1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
① 前4 s内的平均反应速率υ(CO) =______mol·L1·s1。
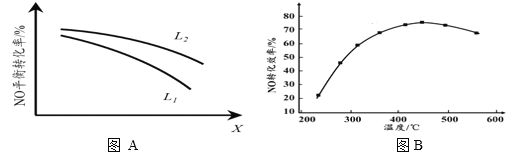
② L、X可分别代表压强或温度。下图A表示L一定时,NO(g)的平衡转化率随X的变化关系。X代表的物理量是______。判断L1、L2的大小关系,并简述理由:______________________________。
(3)实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2) ·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数______(填“>”、“<
②若在2 L的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则k正︰k逆 =___________。(保留一位小数)
II. 有人利用反应C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH = 34.0 kJ·mol1,用活性炭对NO进行吸附。现在密闭容器中加入足量的C和一定量的NO气体并在催化剂作用下发生反应,经相同时间测得NO的转化率随温度的变化如图B所示。由图可知最高转化率对应温度为450℃。低于450℃时,NO的转化率是不是对应温度下的平衡转化率及判断理由是________________________;
N2(g)+CO2(g) ΔH = 34.0 kJ·mol1,用活性炭对NO进行吸附。现在密闭容器中加入足量的C和一定量的NO气体并在催化剂作用下发生反应,经相同时间测得NO的转化率随温度的变化如图B所示。由图可知最高转化率对应温度为450℃。低于450℃时,NO的转化率是不是对应温度下的平衡转化率及判断理由是________________________;