题目内容
2.下列叙述不正确的是( )| A. | 电能是二次能源 | B. | 水力是一次能源 | ||
| C. | 天然气是一次能源 | D. | 蒸汽是一次能源 |
分析 自然界中以现成形式提供的能源称为一次能源,需依靠其他能源间接制取的称为二次能源,据此进行分析判断即可.
解答 解:A.电能是靠其它形式的能量转化而来的,如火力发电,是二次能源,故A正确;
B.水力是自然界中以现成形式提供的能源,是一次能源,故B正确;
C.天然气是古代生物的遗骸经复杂变化而形成的化石燃料,是自然界中以现成形式提供的能源,是一次能源,故C正确;
D.蒸汽是其他能源转化得到的,是二级能源,故D错误;
故选D.
点评 本题主要考查一级能源和二级能源的定义,题目难度不大,注意基础知识的积累.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
10.下列有关物质的性质或用途的叙述中,错误的是( )
| A. | 硅晶体是一种重要的半导体材料 | |
| B. | 石墨可用做绝缘材料 | |
| C. | 漂白粉的有效成分是次氯酸钙 | |
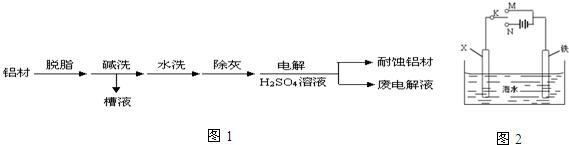
| D. | 常温下,运输浓硫酸、浓硝酸时可用铝制或铁制槽车 |
17.下列元素中,金属性最强的是( )
| A. | 钾 | B. | 钠 | C. | 镁 | D. | 铝 |
7.工业制硫酸中的一步重要反应是SO2在400~600℃下的催化氧化:2SO2+O2?2SO3,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下述有关说法中错误的是( )
| A. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| B. | 在上述条件下,SO2不可能100%地转化为SO3 | |
| C. | 无论怎样控制反应条件,2 mol SO2与1 mol O2 反应时都不会生成2 mol SO3 | |
| D. | 达到平衡时,SO2的浓度与SO3的浓度相等 |
14.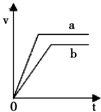 取两份10mL 1mol•L-1稀盐酸,向其中一份中加入过量的锌粒,得到气体的体积随时间变化如b所示,向另一份中加入过量的锌粒同时加入另一种物质,得到气体的体积如a所示,则另一种物质是( )
取两份10mL 1mol•L-1稀盐酸,向其中一份中加入过量的锌粒,得到气体的体积随时间变化如b所示,向另一份中加入过量的锌粒同时加入另一种物质,得到气体的体积如a所示,则另一种物质是( )
 取两份10mL 1mol•L-1稀盐酸,向其中一份中加入过量的锌粒,得到气体的体积随时间变化如b所示,向另一份中加入过量的锌粒同时加入另一种物质,得到气体的体积如a所示,则另一种物质是( )
取两份10mL 1mol•L-1稀盐酸,向其中一份中加入过量的锌粒,得到气体的体积随时间变化如b所示,向另一份中加入过量的锌粒同时加入另一种物质,得到气体的体积如a所示,则另一种物质是( )| A. | 铝粉 | B. | 3 mol•L-1稀硫酸 | C. | 铁粉 | D. | 氢氧化钠固体 |
12. BaS是一种白色晶体,微溶于水,可用于制备立德粉、Na2S等.工业上可用H2与重晶石(BaS04)在高温下反应制备BaS,热化学方程式为BaS04(s)+4H2(g)?BaS(s)+4H20(g)△H=+xkJ•mol-1(x>0).回答下列问题:
BaS是一种白色晶体,微溶于水,可用于制备立德粉、Na2S等.工业上可用H2与重晶石(BaS04)在高温下反应制备BaS,热化学方程式为BaS04(s)+4H2(g)?BaS(s)+4H20(g)△H=+xkJ•mol-1(x>0).回答下列问题:
(1)在温度和容积不变的条件下,能说明该反应己达到平衡状态的是cd(填字母序号).
a.n(H2)=n(H2O)
b.容器内压强保持不变
c.v正(H2)=v逆(H2O)
d.水蒸气的浓度保持不变
(2)平衡后下列措施既可提高反应速率,又可提高H2的转化率的是b(填字母序号).
a.使用催化剂
b.升高反应体系的温度
c.增大反应容器的体积
d.及时从反应体系中分离出水蒸气
(3)将温度恒定为T℃,向体积为2L的密闭容器中加入一定量的重晶石和H2.在不同时间测得H2的物质的量如下表:
①2t时,n< 1.20(填“>”、“<”或“=”)
②若氢气的平衡转化率为a,则该温度下反应的化学平衡常数K=$\frac{{a}^{4}}{(1-a)^{4}}$(用含a的代数式表示);若测得该反应达到平衡时吸热Q kJ,则x=$\frac{2Q}{a}$(用含a、Q的代数式表示).
(4)为了探究温度、固体反应物的表面积对化学反应速率的影响,某同学在一固定容积的密闭容器中加入一定量的重晶石和H2,设计了下表中的三组实验:
①填写上表中的实验条件:T1=850c1=0.80
②在直角坐标系中画出Ⅰ,Ⅱ两组实验氢气的浓度随时间变化趋势图,并在每条曲线上标明对应的实验编号.
 BaS是一种白色晶体,微溶于水,可用于制备立德粉、Na2S等.工业上可用H2与重晶石(BaS04)在高温下反应制备BaS,热化学方程式为BaS04(s)+4H2(g)?BaS(s)+4H20(g)△H=+xkJ•mol-1(x>0).回答下列问题:
BaS是一种白色晶体,微溶于水,可用于制备立德粉、Na2S等.工业上可用H2与重晶石(BaS04)在高温下反应制备BaS,热化学方程式为BaS04(s)+4H2(g)?BaS(s)+4H20(g)△H=+xkJ•mol-1(x>0).回答下列问题:(1)在温度和容积不变的条件下,能说明该反应己达到平衡状态的是cd(填字母序号).
a.n(H2)=n(H2O)
b.容器内压强保持不变
c.v正(H2)=v逆(H2O)
d.水蒸气的浓度保持不变
(2)平衡后下列措施既可提高反应速率,又可提高H2的转化率的是b(填字母序号).
a.使用催化剂
b.升高反应体系的温度
c.增大反应容器的体积
d.及时从反应体系中分离出水蒸气
(3)将温度恒定为T℃,向体积为2L的密闭容器中加入一定量的重晶石和H2.在不同时间测得H2的物质的量如下表:
| 时间/min | 0 | t | 2t | 3t | 4t |
| n(H2)/mol | 2.00 | 1.50 | n | 0.90 | 0.80 |
②若氢气的平衡转化率为a,则该温度下反应的化学平衡常数K=$\frac{{a}^{4}}{(1-a)^{4}}$(用含a的代数式表示);若测得该反应达到平衡时吸热Q kJ,则x=$\frac{2Q}{a}$(用含a、Q的代数式表示).
(4)为了探究温度、固体反应物的表面积对化学反应速率的影响,某同学在一固定容积的密闭容器中加入一定量的重晶石和H2,设计了下表中的三组实验:
| 试验编号 | T/℃ | c起始(H2)/mol•L-1 | 重晶石的比表面积/m2•g-1 |
| Ⅰ | 850 | c1 | 3.4 |
| Ⅱ | T1 | 0.80 | 7.6 |
| Ⅲ | 900 | 0.80 | 7.6 |
②在直角坐标系中画出Ⅰ,Ⅱ两组实验氢气的浓度随时间变化趋势图,并在每条曲线上标明对应的实验编号.
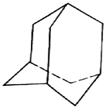 有的油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:
有的油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示: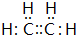 ;
;